ゾコーバ錠125mg
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
医薬品コード(YJコード):62500B8F1020
- 収載区分
- 未収載
- 先発・後発情報
- その他
- オーソライズド
ジェネリック - -
- 一般名
- エンシトレルビル フマル酸錠
- 英名(商品名)
- Xocova
- 規格
- 125mg1錠
- 薬価
- 0.00
- メーカー名
- 塩野義製薬
- 規制区分
- 劇薬
- 長期投与制限
- -
- 標榜薬効
- 抗SARSコロナウイルス2(SARS−CoV−2)薬〔3CLプロテアーゼ阻害薬〕
- 色
- 白〜淡黄白
- 識別コード
- (本体)@ 711 (本体)125 (被包)125mg (被包)@ 711 125
- [@: メーカーロゴ]
- 添付文書
-
PDF 2024年3月改訂(第11版)
- 告示日
- -
- 経過措置期限
- -
- 医薬品マスタに反映
- 2022年12月版
- DIRに反映
- 2023年1月版
- DIR削除予定
- 2024年10月版
- 運転注意
- 情報なし(使用の適否を判断するものではありません)
- ドーピング
- 禁止物質なし(使用の適否を判断するものではありません)
- CP換算
- -
[識別コードの表記 @: メーカーロゴ]
効能効果
SARS-CoV-2による感染症。
(効能又は効果に関連する注意)
5.1. 本剤の投与対象については最新のガイドラインを参考にすること。
5.2. 「17.臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、本剤の使用の必要性を慎重に検討すること〔17.1.1参照〕。
5.3. 重症度の高いSARS-CoV-2による感染症患者に対する有効性は検討されていない。
用法用量
通常、12歳以上の小児及び成人にはエンシトレルビルとして1日目は375mgを、2日目から5日目は125mgを1日1回経口投与する。
(用法及び用量に関連する注意)
SARS-CoV-2による感染症の症状が発現してから72時間以内に投与を開始すること(臨床試験において、症状発現から72時間経過後に投与を開始した患者における有効性を裏付けるデータは得られていない)〔17.1.1参照〕。
外形画像



改訂情報
2024年4月11日 DSU No.325 【その他】
【特殊記載項目】(削除)
【新様式】
本剤は、本邦で緊急承認されたものであり、承認時において有効性及び安全性に係る情報は限られており、引き続き情報を収集中である。そのため、本剤の使用に当たっては、あらかじめ患者又は代諾者に、その旨並びに有効性及び安全性に関する情報を十分に説明し、文書による同意を得てから投与すること。
【7.用法及び用量に関連する注意】(一部改訂)
【新様式】
SARS-CoV-2による感染症の症状が発現してから72時間以内に投与を開始すること。臨床試験において、症状発現から72時間経過後に投与を開始した患者における有効性を裏付けるデータは得られていない。
【9.2腎機能障害患者】(削除)
【新様式】
腎機能障害患者を対象とした臨床試験は実施していない。
【9.3肝機能障害患者】(削除)
【新様式】
肝機能障害患者を対象とした臨床試験は実施していない。
【9.3肝機能障害患者】(一部改訂)
【新様式】
重度の肝機能障害患者(コルヒチンを投与中の患者を除く):
重度の肝機能障害患者を対象とした臨床試験は実施していない。
【9.3肝機能障害患者】(削除)
【新様式】
中等度の肝機能障害患者(コルヒチンを投与中の患者を除く):
本剤の血中濃度が上昇するおそれがある。
【10.2併用注意】(一部改訂)
【新様式】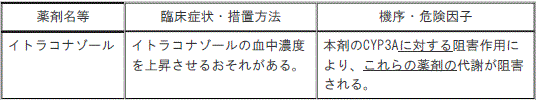
2023年8月3日 DSU No.319 【重要】
【11.1重大な副作用】(新設)
【新様式】
アナフィラキシー
2023年7月20日 使用上の注意改訂情報 令和5年7月20日指示分
【11. 副作用-11.1 重大な副作用】(新設)
【新記載要領】
アナフィラキシー
2023年6月27日 DSU No.318 【その他】
【9.4生殖能を有する者】(一部改訂)
【新様式】
妊娠する可能性のある女性には、本剤投与中及び最終投与後2週間において避妊する必要性及び適切な避妊法について説明すること。
よく一緒に見られている薬
医師の処方により使用する医薬品。


