ネオキシテープ73.5mg
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
医薬品コード(YJコード):2590700S1025
- 収載区分
- 銘柄別収載
- 先発・後発情報
- 先発品(後発品なし)
- オーソライズド
ジェネリック - -
- 一般名
- オキシブチニン塩酸塩貼付剤
- 英名(商品名)
- Neoxy
- 規格
- 73.5mg1枚
- 薬価
- 121.10
- メーカー名
- 久光製薬
- 規制区分
- -
- 長期投与制限
- -
- 標榜薬効
- 排尿障害治療薬〔抗コリン薬〕
- 色
- 半透明(膏体)/淡褐〜褐(支持体)
- 識別コード
- (本体)ネオキシテープ 73.5mg (被包)@ NEOXY Tapes 73.5mg (被包)Hisamitsu NEOXY Tapes 73.5mg (被包)HP3191T
- [@: メーカーロゴ]
- 添付文書
-
PDF 2020年3月改訂(第1版)
- 告示日
- 2013年5月24日
- 経過措置期限
- -
- 医薬品マスタに反映
- 2013年6月版
- 医薬品マスタ削除予定
- -
- 運転注意
-
注意情報あり(使用の適否を判断するものではありません)注意
- ドーピング
- 禁止物質なし(使用の適否を判断するものではありません)
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
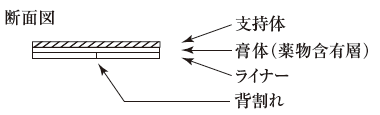
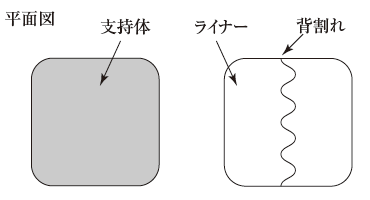
外形画像
改訂情報
-
効能効果
過活動膀胱における尿意切迫感、頻尿及び切迫性尿失禁。
(効能又は効果に関連する注意)
5.1. 本剤を適用する際、十分な問診により臨床症状を確認するとともに類似症状を呈する疾患(尿路感染症、尿路結石、膀胱癌や前立腺癌等の下部尿路における新生物等)に留意し尿検査等により除外診断を実施し必要に応じて専門的な検査も考慮すること。
5.2. 下部尿路閉塞疾患(前立腺肥大症等)を合併している患者では、それに対する治療を優先させること。
5.3. 過活動膀胱の症状を明確に認識できない認知症又は過活動膀胱の症状を明確に認識できない認知機能障害患者は本剤の使用対象とはならない。
用法用量
通常、成人に対し本剤1日1回、1枚(オキシブチニン塩酸塩として73.5mg)を下腹部、腰部又は大腿部のいずれかに貼付し、24時間毎に貼り替える。
警告・禁忌・相互作用・その他の注意
(禁忌)
2.1. 尿閉を有する患者[抗コリン作用により排尿時の膀胱収縮が抑制され、症状が悪化するおそれがある]〔11.1.3参照〕。
2.2. 閉塞隅角緑内障の患者[抗コリン作用により眼圧が上昇し、症状が悪化するおそれがある]。
2.3. 重篤な心疾患のある患者[抗コリン作用により頻脈、心悸亢進を起こし心臓の仕事量が増加するおそれがある]。
2.4. 幽門閉塞、十二指腸閉塞又は腸管閉塞している患者及び麻痺性イレウスのある患者[抗コリン作用により胃腸の平滑筋の収縮及び運動が抑制され、症状が悪化するおそれがある]〔11.1.2参照〕。
2.5. 胃アトニー又は腸アトニーのある患者[抗コリン作用により消化管運動が低下するため症状が悪化するおそれがある]。
2.6. 重症筋無力症の患者[抗コリン作用により筋緊張の低下がみられ症状が悪化するおそれがある]。
2.7. 本剤の成分に対し過敏症の既往歴のある患者。
2.8. 授乳婦〔9.6授乳婦の項参照〕。
(重要な基本的注意)
8.1. 眼調節障害(視力障害、霧視等)、めまい、眠気があらわれることがあるので、本剤使用中の患者には、自動車の運転等、危険を伴う機械の操作に注意させること。
8.2. 前立腺肥大症等の下部尿路閉塞疾患を有する患者に対しては、本剤使用前に残尿量測定を実施し、必要に応じて、専門的な検査をし、使用後は残尿量の増加に注意し、十分な経過観察を行うこと〔9.1.1、11.1.3参照〕。
8.3. 本剤使用により効果が認められない場合には、漫然と使用せず、適切な治療を考慮すること。
8.4. 本剤の貼付により皮膚症状があらわれることがある。皮膚刺激及び皮膚の角質層剥離等による血中濃度の上昇を避けるため、貼付箇所を毎回変更すること。皮膚症状があらわれた場合には、ステロイド外用剤又は抗ヒスタミン外用剤等を使用するか、本剤の一時休薬又は使用を中止するなど適切な処置を行うこと〔11.2参照〕。
8.5. 抗コリン作用により発汗抑制が起こり、外部の温度上昇に対する不耐性が生じて、急激に体温が上昇するおそれがあるため、高温環境下で使用する場合は体温上昇に注意させること。
(特定の背景を有する患者に関する注意)
(合併症・既往歴等のある患者)
9.1.1. 下部尿路閉塞疾患(前立腺肥大症等)を合併している患者:抗コリン作用により、尿閉を誘発するおそれがある〔8.2、11.1.3参照〕。
9.1.2. 甲状腺機能亢進症の患者:抗コリン作用により、頻脈等の交感神経興奮症状が悪化するおそれがある。
9.1.3. うっ血性心不全の患者:代償性交感神経系の亢進を更に亢進させるおそれがある。
9.1.4. 不整脈のある患者:頻脈性不整脈を有している患者では、副交感神経遮断作用により交感神経が優位にたち、心拍数増加等が起こるおそれがある。
9.1.5. 潰瘍性大腸炎の患者:中毒性巨大結腸があらわれるおそれがある。
9.1.6. パーキンソン症状又は脳血管障害のある患者:症状の悪化あるいは精神神経症状があらわれるおそれがある。
9.1.7. 認知症又は認知機能障害のある患者:抗コリン作用により、症状が悪化するおそれがある。
(腎機能障害患者)
9.2.1. 重篤な腎障害のある患者:腎排泄が遅延するおそれがある。
(肝機能障害患者)
9.3.1. 重篤な肝障害のある患者:主として肝で代謝されるため、副作用が発現しやすくなるおそれがある〔16.4参照〕。
(妊婦)
妊婦又は妊娠している可能性のある女性には使用しないことが望ましい。
(授乳婦)
授乳を避けさせること(動物実験(ラット)で乳汁への移行が報告されている)〔2.8参照〕。
(小児等)
小児等を対象とした臨床試験は実施していない。
(高齢者)
一般に、生理機能が低下している。
(相互作用)
本剤は、主として肝の薬物代謝酵素CYP3A4により代謝される〔16.4参照〕。
10.2. 併用注意:
1). 抗コリン作用を有する薬剤、三環系抗うつ剤、フェノチアジン系薬剤、モノアミン酸化酵素阻害剤[口内乾燥、便秘、排尿困難等があらわれるおそれがある(抗コリン作用が増強されるおそれがある)]。
2). CYP3A4を阻害する薬剤(ケトコナゾール、イトラコナゾール等)[口内乾燥、便秘、排尿困難等があらわれるおそれがある(これらの薬剤はCYP3A4を強力に阻害し、併用により本剤の血中濃度が上昇する可能性がある)]。
(過量投与)
13.1. 症状
過量投与時、尿閉、散瞳、興奮、頻脈等。
13.2. 処置
過量投与時、本剤を貼付している場合には、直ちに本剤を剥離すること。過量投与時の尿閉に対しては導尿等、過量投与時の散瞳に対してはピロカルピン投与等、各症状に応じて適切な処置を行うこと。
(適用上の注意)
14.1. 薬剤交付時の注意
14.1.1. 貼付部位
(1). 衣服との摩擦ではがれるおそれがあるため、ベルトラインを避けること。
(2). 創傷面又は湿疹・皮膚炎等がみられる部位は避けて貼付すること。
(3). 貼付部位の皮膚を拭い、清潔な皮膚に本剤を貼付すること。また、貼付部位の水分は十分に取り除くこと。
14.1.2. 貼付時
(1). 本剤を使用する際には、ライナーを剥がして使用すること。
(2). 本剤は1日毎に貼り替えるため、貼付開始時刻の設定にあたっては入浴等の時間を考慮することが望ましい。
14.1.3. 貼り替え時
(1). 本剤を剥離する際は皮膚の損傷を避けるため、ゆっくりと慎重に剥離すること。
(2). 本剤が途中ではがれ落ちた場合は、直ちに新たな本剤を貼付し、また、次の貼り替え予定時間には新たな本剤に貼り替えること。
(3). 貼付箇所を毎回変更し、繰り返し同一箇所には貼付しないこと。
(4). 貼付24時間後も本剤の成分が残っているので、使用済みの製剤は接着面を内側にして折りたたみ、小児の手及び目の届かない所に安全に廃棄すること。
14.1.4. 保管時
(1). 本剤を小児の手の届かない場所に保管すること。
(2). 高温を避けて保管すること。
(3). 開封後はチャックを閉め密封して保管し、開封日より14日を超えたものは使用しないこと。
(保管上の注意)
室温保存。
副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には使用を中止するなど適切な処置を行うこと。
11.1. 重大な副作用
11.1.1. 血小板減少(頻度不明)。
11.1.2. 麻痺性イレウス(頻度不明):著しい便秘、腹部膨満等があらわれた場合には使用を中止し、適切な処置を行うこと〔2.4参照〕。
11.1.3. 尿閉(頻度不明)〔2.1、8.2、9.1.1参照〕。
11.2. その他の副作用
1). 消化器:(5%以上)口内乾燥、(0.1%以上5%未満)便秘、上腹部痛、胃炎、下痢、口内炎、口唇炎、消化不良、腹痛。
2). 精神神経系:(0.1%以上5%未満)傾眠、浮動性めまい。
3). 泌尿器・腎臓:(0.1%以上5%未満)排尿困難、膀胱炎、残尿、尿中蛋白陽性、尿中白血球陽性、尿中赤血球陽性。
4). 皮膚:(5%以上)*適用部位皮膚炎(46.6%)、(0.1%以上5%未満)*適用部位紅斑、*適用部位そう痒感、*適用部位湿疹、発汗障害。
5). 循環器:(0.1%以上5%未満)心室性期外収縮。
6). 過敏症:(0.1%以上5%未満)じん麻疹、湿疹。
7). 肝臓:(0.1%以上5%未満)AST上昇、ALT上昇、γ-GTP上昇、血中ビリルビン上昇、尿中ウロビリノーゲン上昇。
8). 血液:(0.1%以上5%未満)好酸球増加、単球増加、白血球数増加、白血球数減少、リンパ球減少、好中球増加、好中球減少、好塩基球増加、血小板数増加。
9). その他:(0.1%以上5%未満)倦怠感、LDH増加、LDH減少、血中コレステロール増加、(頻度不明)浮腫。
*)〔8.4参照〕。
薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男女に本剤(オキシブチニン塩酸塩として73.5mg)を下腹部に24時間単回貼付したとき、オキシブチニン及び活性代謝物であるN-デスエチルオキシブチニン(DEO)の血漿中濃度はそれぞれ貼付後18.0及び24.0時間に最高に達し、Cmaxはそれぞれ5.2及び5.0ng/mLであった。また、剥離後の半減期はそれぞれ15.3及び15.4時間であった。
オキシブチニン及びDEOの血漿中濃度推移(下腹部貼付時)(平均値±標準偏差)
<<図省略>>
薬物動態パラメータ(下腹部貼付時)
<<表省略>>
本剤を腰部及び大腿部に貼付したとき、オキシブチニンのAUC0-tは下腹部貼付時に比べ腰部で約1.37倍、大腿部で約1.48倍に上昇した。
16.1.2 反復投与(健康成人)
健康成人男性にオキシブチニン塩酸塩52.5及び105mg注)を含有する経皮製剤を下腹部に1日1回7日間反復貼付したとき、オキシブチニン及びDEOの薬物動態パラメータ(AUC0-23.5及びCmax)は、52.5mgと105mgとの間で線形であると考えられた。また、反復貼付時は2回目貼付時よりほぼ定常状態に達していると考えられた。
貼付7回目の薬物動態パラメータ
<<表省略>>
16.1.3 反復投与(過活動膀胱患者)
過活動膀胱患者に本剤(オキシブチニン塩酸塩として73.5mg)を下腹部、腰部、大腿部のいずれかに1日1回52週間反復貼付したときの平均血漿中オキシブチニン及びDEO濃度は、貼付後12、28及び52週でそれぞれほぼ一定であった。また、過活動膀胱患者における血漿中濃度はおおむね健康成人における単回貼付時の薬物動態から予測される範囲内であったことから、健康成人と過活動膀胱患者の体内動態は大きく異ならないと考えられた。
16.3 分布
16.3.1 組織分布
SD系雄性ラットの背部皮膚に[14C]オキシブチニン塩酸塩を含有する経皮製剤を48時間単回貼付したとき、放射能は組織に広く分布し、その中で特に貼付部位皮膚、ハーダー腺、白色脂肪及び肝臓で高濃度を示した。製剤剥離後、各組織の放射能濃度は血漿中放射能濃度と同様に減少した。また、反復貼付による投与部位皮膚への蓄積性も認められなかった。
16.3.2 胎児移行
妊娠ラットに[14C]オキシブチニン塩酸塩を経口投与したとき、胎児の組織中に分布が認められたが、その濃度は母動物の血中濃度より低いことが報告されている。
16.3.3 血漿蛋白結合
In vitro試験において、ヒト血漿蛋白結合率はオキシブチニン及びDEOのいずれも99%以上(血漿中濃度400ng/mL)であることが報告されている。
16.4 代謝
オキシブチニンは主に肝臓で代謝され、活性代謝物であるDEOなどに代謝される。また、ヒト肝ミクロゾームを用いた検討により、オキシブチニンの代謝には主にCYP3A4及びCYP3A5が関与していることが報告されている(in vitro)。[9.3.1、10.参照]
16.5 排泄
健康成人男性にオキシブチニン塩酸塩52.5mg注)を含有する経皮製剤を下腹部に1日1回7日間反復貼付したとき、貼付開始後144~168時間(貼付7回目)の尿中排泄率(オキシブチニン及び4種の代謝物)は、投与量に対して1.4%であった。また、その内訳は3.8%がフェニルシクロヘキシルグリコール酸、30.8%が4-水酸化N-デスエチルオキシブチニン、65.4%が4-水酸化フェニルシクロヘキシルグリコール酸であり、オキシブチニン及びDEOはほとんどみられなかった。105mg注)を含有する経皮製剤貼付時においても同様の傾向が認められた。
注)本剤の承認された用量は73.5mgである。
臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国内第III相試験(二重盲検比較試験)
過活動膀胱患者を対象に本剤1日1回、1枚(オキシブチニン塩酸塩として73.5mg)を12週間貼付した結果、主要評価項目である平均排尿回数の変化量において、プラセボ群に対し有意な改善効果が認められた。また、平均尿意切迫感回数の変化量においても同様にプラセボ群に対し有意な改善効果が認められた。
<<表省略>>
副作用発現頻度はオキシブチニン群で51.2%(293/572例)であった。主な副作用は、適用部位皮膚炎31.8%(182/572例)、口内乾燥6.3%(36/572例)及び適用部位紅斑5.6%(32/572例)であった。
17.1.2 国内第III相試験(長期投与試験)
過活動膀胱患者を対象に本剤1日1回、1枚(オキシブチニン塩酸塩として73.5mg)を52週間貼付した結果、主要評価項目である平均排尿回数の変化量において、貼付前のベースラインに対する改善効果が認められ、その効果は減弱することなく52週間持続した。また、平均尿意切迫感回数及び平均切迫性尿失禁回数の変化量においても同様に貼付前のベースラインに対する改善効果が認められた。
<<表省略>>
副作用発現頻度は83.8%(362/432例)であった。主な副作用は、適用部位皮膚炎73.8%(319/432例)、口内乾燥9.7%(42/432例)及び好酸球百分率増加5.6%(24/432例)であった。
薬効薬理
18.1 作用機序
オキシブチニン塩酸塩は、向神経作用(抗ムスカリン作用)に加え、平滑筋直接弛緩作用(カルシウム拮抗作用)を有し、膀胱に協力的に作用することにより、膀胱の過緊張状態を抑制すると考えられている。
18.2 ムスカリン受容体に対する親和性
ヒトムスカリン受容体(M1、M2、M3、M4及びM5)を用いた結合実験において、オキシブチニンは[3H]N-メチルスコポラミン結合を競合的に阻害し、ムスカリンM3及びM4受容体に対して高い親和性を示した(in vitro)。
18.3 摘出平滑筋に対する作用
ラット、モルモット及びヒトの摘出膀胱平滑筋を用いた試験で、オキシブチニンはアセチルコリン及びカルバコールによる収縮を抑制し(抗コリン作用)、また、高用量でカリウム収縮を抑制した(カルシウム拮抗作用)。代謝物であるDEOはオキシブチニンと同様に抗コリン作用及び膀胱平滑筋直接作用(カルシウム拮抗作用)を示した(in vitro)。
18.4 排尿機能に対する作用
ラットの膀胱内圧測定試験(シストメトリー)において、本剤は用量依存的に排尿までの時間を延長させた。
類似した薬効の薬
よく一緒に見られている薬
医師の処方により使用する医薬品。



 で医薬品を比較する
で医薬品を比較する
