ボリコナゾール顆粒20%「タカタ」
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
医薬品コード(YJコード):6179001D1022
- 収載区分
- 銘柄別収載
- 先発・後発情報
- 後発品(加算対象)
- オーソライズド
ジェネリック - -
- 一般名
- ボリコナゾール顆粒
- 英名(商品名)
- Voriconazole TAKATA
- 規格
- 20%1g
- 薬価
- 2,624.90
- メーカー名
- 高田製薬
- 規制区分
- 劇薬
- 長期投与制限
- -
- 標榜薬効
- 抗真菌薬〔トリアゾール系抗菌薬〕
- 色
- 黄白
- 識別コード
- -
- [@: メーカーロゴ]
- 添付文書
-
PDF 2025年10月改訂(第5版)
- 告示日
- 2024年12月5日
- 経過措置期限
- -
- 医薬品マスタに反映
- 2025年1月版
- 医薬品マスタ削除予定
- -
- 運転注意
-
禁止情報あり(使用の適否を判断するものではありません)禁止
- ドーピング
- 禁止物質なし(使用の適否を判断するものではありません)
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
改訂情報
2025年11月5日 DSU No.340 【その他】
【2.禁忌】(一部改訂)
次の薬剤を投与中の患者:リファンピシン、リファブチン、エファビレンツ、リトナビル、ロピナビル・リトナビル、ニルマトレルビル・リトナビル、カルバマゼピン、バルビタール、フェノバルビタール、ピモジド、キニジン、イバブラジン、麦角アルカロイド(エルゴタミン・無水カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン)、トリアゾラム、チカグレロル、アスナプレビル、ロミタピド、ブロナンセリン、スボレキサント、リバーロキサバン、アゼルニジピン、オルメサルタンメドキソミル・アゼルニジピン、ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期)、アナモレリン、ルラシドン、イサブコナゾニウム、フィネレノン、エプレレノン、ボクロスポリン、マバカムテン
【10.1併用禁忌】(追記)
2025年6月3日 DSU No.336 【重要】
【2.禁忌】(一部改訂)
次の薬剤を投与中の患者:リファンピシン、リファブチン、エファビレンツ、リトナビル、ロピナビル・リトナビル、ニルマトレルビル・リトナビル、カルバマゼピン、バルビタール、フェノバルビタール、ピモジド、キニジン、イバブラジン、麦角アルカロイド(エルゴタミン・無水カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン)、トリアゾラム、チカグレロル、アスナプレビル、ロミタピド、ブロナンセリン、スボレキサント、リバーロキサバン、アゼルニジピン、オルメサルタンメドキソミル・アゼルニジピン、ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期)、アナモレリン、ルラシドン、イサブコナゾニウム、フィネレノン、エプレレノン
【10.1併用禁忌】(削除)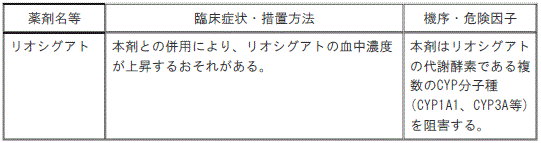
【10.1併用禁忌】(追記)
【10.2併用注意】(追記)
2025年6月3日 DSU No.336 【その他】
【2.禁忌】(一部改訂)
次の薬剤を投与中の患者:リファンピシン、リファブチン、エファビレンツ、リトナビル、ロピナビル・リトナビル、ニルマトレルビル・リトナビル、カルバマゼピン、バルビタール、フェノバルビタール、ピモジド、キニジン、イバブラジン、麦角アルカロイド(エルゴタミン・無水カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン)、トリアゾラム、チカグレロル、アスナプレビル、ロミタピド、ブロナンセリン、スボレキサント、リバーロキサバン、アゼルニジピン、オルメサルタンメドキソミル・アゼルニジピン、ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期)、アナモレリン、ルラシドン、イサブコナゾニウム、フィネレノン、エプレレノン、ボクロスポリン
【10.1併用禁忌】(追記)
2025年5月20日 使用上の注意改訂情報 令和7年5月20日指示分
【2. 禁忌(次の患者には投与しないこと)】(一部改訂)
次の薬剤を投与中の患者:リファンピシン、リファブチン、エファビレンツ、リトナビル、ロピナビル・リトナビル、ニルマトレルビル・リトナビル、カルバマゼピン、バルビタール、フェノバルビタール、ピモジド、キニジン、イバブラジン、麦角アルカロイド(エルゴタミン・無水カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン)、トリアゾラム、チカグレロル、アスナプレビル、ロミタピド、ブロナンセリン、スボレキサント、リバーロキサバン、アゼルニジピン、オルメサルタン メドキソミル・アゼルニジピン、ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期)、アナモレリン、ルラシドン、イサブコナゾニウム、フィネレノン、エプレレノン
【10. 相互作用-10.1 併用禁忌(併用しないこと)】(削除)
【10. 相互作用-10.1 併用禁忌(併用しないこと)】(新設)
【10. 相互作用-10.2 併用注意(併用に注意すること)】(新設)
効能効果
1). 次記の重症又は難治性真菌感染症:
・ 侵襲性アスペルギルス症、肺アスペルギローマ、慢性壊死性肺アスペルギルス症。
・ カンジダ血症、食道カンジダ症、カンジダ腹膜炎、気管支カンジダ症・肺カンジダ症。
・ クリプトコックス髄膜炎、肺クリプトコックス症。
・ フサリウム症。
・ スケドスポリウム症。
2). 造血幹細胞移植患者における深在性真菌症の予防。
(効能又は効果に関連する注意)
5.1. 〈カンジダ感染の治療〉他の抗真菌剤が無効あるいは忍容性に問題があると考えられる場合に本剤の使用を考慮すること。
5.2. 〈造血幹細胞移植患者における深在性真菌症の予防〉真菌感染に高リスクの患者(好中球数が500/mm3未満に減少することが予測される患者など)を対象とすること。
用法用量
1). 成人(体重40kg以上):通常、ボリコナゾールとして初日は1回300mg(顆粒剤として1.5g)を1日2回、2日目以降は1回150mg(顆粒剤として0.75g)又は1回200mg(顆粒剤として1g)を1日2回食間に経口投与する。なお、患者の状態に応じて、又は効果不十分の場合には、増量できるが、初日投与量の上限は1回400mg(顆粒剤として2g)1日2回、2日目以降投与量の上限は1回300mg1日2回までとする。
2). 成人(体重40kg未満):通常、ボリコナゾールとして初日は1回150mgを1日2回、2日目以降は1回100mg(顆粒剤として0.5g)を1日2回食間に経口投与する。なお、患者の状態に応じて、又は効果不十分の場合には2日目以降の投与量を1回150mg1日2回まで増量できる。
3). 小児(2歳以上12歳未満及び12歳以上で体重50kg未満):ボリコナゾール注射剤による投与を行った後、通常、ボリコナゾールとして1回9mg/kg(顆粒剤として45mg/kg)を1日2回食間に経口投与する。なお、患者の状態に応じて、又は効果不十分の場合には1mg/kg(顆粒剤として5mg/kg)ずつ増量し、忍容性が不十分の場合には1mg/kgずつ減量する(最大投与量として350mg(顆粒剤として1.75g)を用いた場合は50mg(顆粒剤として0.25g)ずつ減量する)。
ただし、1回350mg1日2回を上限とする。
4). 小児(12歳以上で体重50kg以上):ボリコナゾール注射剤による投与を行った後、通常、ボリコナゾールとして1回200mgを1日2回食間に経口投与する。なお、患者の状態に応じて、又は効果不十分の場合には1回300mg1日2回まで増量できる。
(用法及び用量に関連する注意)
7.1. 〈効能共通〉注射剤からボリコナゾールの投与を開始した成人患者において、経口投与可能であると医師が判断した場合は、錠剤、顆粒又はドライシロップに切り替えることができる。
7.2. 〈効能共通〉小児においては、注射剤からボリコナゾールの投与を開始し、患者の状態に応じて、経口投与可能であると医師が判断した場合に、錠剤、顆粒又はドライシロップに切り替えることができるが、投与開始から1週間未満で注射剤から経口剤に変更した際の有効性及び安全性は検討されていないため慎重に判断すること。なお、ボリコナゾール注射剤では食道カンジダ症の適応はないため、小児の食道カンジダ症に対する本剤の使用は推奨されない〔16.1.2参照〕。
7.3. 〈効能共通〉腎機能障害のある患者で注射剤の投与ができない成人患者に対しては、錠剤、顆粒又はドライシロップを使用すること。
7.4. 〈効能共通〉軽度~中等度肝機能低下(Child Pugh分類クラスA・Bの肝硬変に相当)がある患者では投与初日は通常の初日投与量とし、2日目以降は通常の2日目以降投与量の半量とすること〔9.3.2、15.1.1、16.6.1参照〕。
7.5. 〈造血幹細胞移植患者における深在性真菌症の予防〉好中球数が500/mm3以上に回復する、又は免疫抑制剤の投与終了など、適切な時期に投与を終了すること(臨床試験において、180日を超えた投与の有効性及び安全性は検討されていない)。
警告・禁忌・相互作用・その他の注意
(警告)
1.1. 本剤による治療にあたっては、感染症の治療に十分な知識と経験を持つ医師又はその指導のもとで、重症又は難治性の真菌感染症患者を対象に行うこと。
1.2. 重篤な肝障害があらわれることがあるので、投与にあたっては、観察を十分に行い、肝機能検査を定期的に行うこと(異常が認められた場合には投与を中止し、適切な処置を行うこと)〔8.2、11.1.3参照〕。
1.3. 羞明、霧視、視覚障害等の症状があらわれ、本剤投与中止後も症状が持続することがある。本剤投与中及び投与中止後もこれらの症状が回復するまでは、自動車の運転等危険を伴う機械の操作には従事させないように十分注意すること〔8.5、11.2参照〕。
(禁忌)
2.1. 次の薬剤を投与中の患者:リファンピシン投与中、リファブチン投与中、エファビレンツ投与中、リトナビル投与中、ロピナビル・リトナビル投与中、ニルマトレルビル・リトナビル投与中、カルバマゼピン投与中、バルビタール投与中、フェノバルビタール投与中、ピモジド投与中、キニジン投与中、イバブラジン投与中、麦角アルカロイド投与中(エルゴタミン・無水カフェイン・イソプロピルアンチピリン、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン)、トリアゾラム投与中、チカグレロル投与中、アスナプレビル投与中、ロミタピド投与中、ブロナンセリン投与中、スボレキサント投与中、リバーロキサバン投与中、アゼルニジピン投与中、オルメサルタン メドキソミル・アゼルニジピン投与中、ベネトクラクス<再発又は難治性の慢性リンパ性白血病の用量漸増期>投与中(ベネトクラクス<再発又は難治性の小リンパ球性リンパ腫の用量漸増期>投与中を含む)、アナモレリン投与中、ルラシドン投与中、イサブコナゾニウム投与中、フィネレノン投与中、エプレレノン投与中、ボクロスポリン投与中、マバカムテン投与中〔10.1参照〕。
2.2. 本剤の成分に対して過敏症の既往歴のある患者。
2.3. 妊婦又は妊娠している可能性のある患者〔9.5妊婦の項参照〕。
(重要な基本的注意)
8.1. 重篤な血液障害、重篤な腎障害、高カリウム血症があらわれることがあるので、本剤の投与に際しては定期的に血液検査、腎機能検査、血中電解質検査を行うなど観察を十分に行うこと〔11.1.6、11.1.9、11.1.16参照〕。
8.2. 重篤な肝障害があらわれることがあるので、本剤の投与に際しては、観察を十分に行い、必要に応じて肝機能検査を定期的(月に1~2回)に行うこと〔1.2、11.1.3参照〕。
8.3. 心電図QT延長、心室頻拍(torsade de pointesを含む)、心室細動、不整脈、完全房室ブロック、心室性二段脈、心室性期外収縮、頻脈等があらわれることがあるので、定期的に心電図検査を行うなど観察を十分に行うこと〔9.1.2、11.1.4参照〕。
8.4. 本剤の投与に際しては、アレルギー既往歴、薬物過敏症等について十分な問診を行うこと。
8.5. 視神経炎、視神経乳頭浮腫等の眼障害があらわれ投与中止後も羞明、霧視、視覚障害等の症状が持続することがあるので投与中及び投与中止後も症状が回復するまでは自動車の運転等危険を伴う機械の操作には従事させないように十分注意すること。また、視神経炎、視神経乳頭浮腫等の眼障害があらわれ、本剤投与中止後も羞明、霧視、視覚障害等の症状が持続することがあるので、本剤を投与する患者にはあらかじめ説明し、必要に応じて眼科専門医を受診するよう指導すること〔1.3、11.2参照〕。
8.6. 光線過敏性反応があらわれることがあるので、本剤投与中は長袖の衣服、帽子等の着用により日光の照射を避け、日焼け止め効果の高いサンスクリーンの使用により紫外線の照射を避けること。本剤投与中に光線過敏性反応があらわれた場合は、本剤の投与を中止すること(やむを得ず投与を継続する場合は、皮膚科医を定期的に受診するよう指導し、日光角化症などの前癌病変の早期発見に留意すること)〔15.1.3参照〕。
8.7. 投与期間中は血中濃度をモニタリングすることが望ましい〔15.1.1参照〕。
8.8. 本剤投与開始にあたっては、あらかじめワルファリン服用の有無を確認し、ワルファリンと併用する場合は、プロトロンビン時間測定及びトロンボテストの回数を増やすなど慎重に投与すること〔10.2参照〕。
8.9. 本剤はCYP3Aに対する強い阻害作用を有するため、患者の併用薬剤に注意し、併用薬にCYP3Aにより薬物動態学的相互作用を受けやすい薬剤(「10.2併用注意」の項に記載されていない薬剤も含む)が含まれている場合は、必要に応じて併用薬の減量を考慮するなど慎重に投与すること〔10.相互作用の項、16.4参照〕。
(特定の背景を有する患者に関する注意)
(合併症・既往歴等のある患者)
9.1.1. 薬物過敏症の既往歴のある患者(ただし、本剤に対して過敏症の既往歴のある患者には投与しないこと)。
9.1.2. 不整脈を有する患者及び不整脈を発現しやすい状態にある患者:投与前に電解質異常(カリウム、マグネシウム、カルシウム)を補正すること。また、本剤と電解質異常を生じさせる可能性のある血液製剤を同時に投与しないこと〔8.3、11.1.4参照〕。
(肝機能障害患者)
9.3.1. 重度肝機能低下(Child Pugh分類クラスCの肝硬変に相当)のある患者:定期的に検査を行うなど観察を十分に行うこと(薬物動態、安全性は検討されていない)。
9.3.2. 軽度~中等度肝機能低下(Child Pugh分類クラスA・Bの肝硬変に相当)のある患者〔7.4、16.6.1参照〕。
(妊婦)
妊婦又は妊娠している可能性のある女性には投与しないこと(ラット10mg/kg以上投与において催奇形性(口蓋裂、水腎症/尿管水腫)、ウサギ100mg/kg投与において胎仔毒性(胎仔死亡率増加、胎仔骨格変異等)が認められた)〔2.3参照〕。
(授乳婦)
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること(母乳中への移行は不明である)。
(小児等)
9.7.1. 低出生体重児、新生児、乳児又は2歳未満の幼児を対象とした臨床試験は実施していない。
9.7.2. 日光の照射を避けること(皮膚弾力性低下、皮膚色素沈着や皮膚色素脱失等の皮膚光老化が認められた場合は、投与中止後も観察を行うことが望ましい)、小児で光線過敏性反応及び皮膚扁平上皮癌が発現した報告がある。
9.7.3. 投与に際しては観察を十分に行うこと。小児を対象とした海外臨床試験では、成人と比べ肝酵素上昇の発現頻度が高いことが報告されている。
9.7.4. 用量を増減する時には、患者の状態を十分に観察し、効果及び副作用の発現を考慮して、必要最小限の増量又は減量にとどめること(ただし、原則として、投与開始後及び増量後、少なくとも3日間は増量しないこと)。
(高齢者)
用量に留意するなど慎重に投与すること(一般に生理機能が低下している)。
(相互作用)
本剤は、肝代謝酵素CYP2C19、2C9及び3A4で代謝され、CYP2C19、2C9及び3A4の阻害作用を有する(in vitro)。CYP3Aに対する阻害作用は強い〔8.9、16.4参照〕。
10.1. 併用禁忌:
1). リファンピシン<リマクタン、アプテシン、リファジン>〔2.1参照〕[リファンピシンとの併用により、本剤のCmaxは93%・AUCは96%減少した(リファンピシンは、本剤の代謝酵素(CYP3A4)を誘導する)]。
2). リファブチン:
①. リファブチン<ミコブティン>〔2.1参照〕[リファブチンとの併用により、本剤のCmaxは69%・AUCは78%減少した(リファブチンは、本剤の代謝酵素(CYP3A4)を誘導する)]。
②. リファブチン<ミコブティン>〔2.1参照〕[本剤との併用によりリファブチンのCmaxは3.0倍・AUCは4.3倍増加した(本剤はリファブチンの代謝酵素(CYP3A4)を阻害する)]。
3). エファビレンツ:
①. エファビレンツ<ストックリン>〔2.1参照〕[エファビレンツとの併用により、本剤のCmaxは61%・AUCは77%減少した(エファビレンツは、本剤の代謝酵素(CYP2C19及びCYP2C9)を誘導する)]。
②. エファビレンツ<ストックリン>〔2.1参照〕[本剤との併用によりエファビレンツのCmaxは1.4倍・AUCは1.4倍増加した(本剤はエファビレンツの代謝酵素(CYP3A4)を阻害する)]。
4). リトナビル<ノービア>、ロピナビル・リトナビル<カレトラ>、ニルマトレルビル・リトナビル<パキロビッドパック>〔2.1参照〕[リトナビルとの併用により、本剤のCmaxは66%・AUCは82%減少した(リトナビルは、本剤の代謝酵素(CYP2C19及びCYP2C9)を誘導する)]。
5). カルバマゼピン<テグレトール>、長時間作用型バルビツール酸誘導体(バルビタール、フェノバルビタール<フェノバール>)〔2.1参照〕[これらの薬剤との併用により、本剤の代謝が促進され血中濃度が減少するおそれがある(これらの薬剤は、本剤の代謝酵素(CYP3A4)を誘導する)]。
6). ピモジド<オーラップ>、キニジン〔2.1参照〕[本剤との併用により、これらの薬剤の血中濃度が増加し、QT延長、心室性不整脈
7). イバブラジン<コララン>〔2.1参照〕[本剤との併用により、イバブラジンの血中濃度が増加し過度の徐脈があらわれるおそれがある(本剤はイバブラジンの代謝酵素(CYP3A)を阻害する)]。
8). 麦角アルカロイド(エルゴタミン・無水カフェイン・イソプロピルアンチピリン<クリアミン配合錠>、ジヒドロエルゴタミン、エルゴメトリン、メチルエルゴメトリン<パルタンM>)〔2.1参照〕[本剤との併用により、これらの薬剤の血中濃度が増加し麦角中毒を引き起こすおそれがある(本剤はこれら薬剤の代謝酵素(CYP3A4)を阻害する)]。
9). トリアゾラム<ハルシオン>〔2.1参照〕[本剤との併用により、トリアゾラムの血中濃度が増加し作用の増強や作用時間延長を引き起こすおそれがある(本剤はトリアゾラムの代謝酵素(CYP3A4)を阻害する)]。
10). チカグレロル<ブリリンタ>〔2.1参照〕[本剤との併用により、チカグレロルの血中濃度が上昇し血小板凝集抑制作用が増強するおそれがある(本剤はチカグレロルの代謝酵素(CYP3A)を阻害する)]。
11). アスナプレビル<スンベプラ>〔2.1参照〕[本剤との併用により、アスナプレビルの血中濃度が上昇し肝臓に関連した有害事象が発現又は重症化するおそれがある(本剤はアスナプレビルの代謝酵素(CYP3A)を阻害する)]。
12). ロミタピド<ジャクスタピッド>〔2.1参照〕[本剤との併用により、ロミタピドの血中濃度が上昇するおそれがある(本剤はロミタピドの代謝酵素(CYP3A)を阻害する)]。
13). ブロナンセリン<ロナセン>〔2.1参照〕[本剤との併用により、ブロナンセリンの血中濃度が上昇し作用が増強するおそれがある(本剤はブロナンセリンの代謝酵素(CYP3A4)を阻害する)]。
14). スボレキサント<ベルソムラ>〔2.1参照〕[本剤との併用により、スボレキサントの血中濃度が上昇し作用が増強するおそれがある(本剤はスボレキサントの代謝酵素(CYP3A)を阻害する)]。
15). リバーロキサバン<イグザレルト>〔2.1参照〕[本剤との併用により、リバーロキサバンの血中濃度が上昇し抗凝固作用が増強することにより出血の危険性が増大するおそれがある(本剤はリバーロキサバンの代謝酵素(CYP3A4)を阻害する)]。
16). アゼルニジピン<カルブロック>、オルメサルタン メドキソミル・アゼルニジピン<レザルタス>〔2.1参照〕[本剤との併用により、アゼルニジピンの血中濃度が上昇するおそれがある(本剤はアゼルニジピンの代謝酵素(CYP3A4)を阻害する)]。
17). ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の用量漸増期)<ベネクレクスタ>〔2.1参照〕[本剤との併用により、ベネトクラクスの血中濃度が増加し腫瘍崩壊症候群の発現が増強されるおそれがある(本剤はベネトクラクスの代謝酵素(CYP3A)を阻害する)]。
18). アナモレリン<エドルミズ>〔2.1参照〕[本剤との併用により、アナモレリンの血中濃度が増加し副作用の発現が増強されるおそれがある(本剤はアナモレリンの代謝酵素(CYP3A4)を阻害する)]。
19). ルラシドン<ラツーダ>〔2.1参照〕[本剤との併用により、ルラシドンの血中濃度が上昇し作用が増強するおそれがある(本剤はルラシドンの代謝酵素(CYP3A4)を阻害する)]。
20). イサブコナゾニウム<クレセンバ>〔2.1参照〕[本剤との併用により、イサブコナゾールの血中濃度が上昇し作用が増強するおそれがある(本剤はイサブコナゾールの代謝酵素(CYP3A)を阻害する)]。
21). フィネレノン<ケレンディア>〔2.1参照〕[本剤との併用により、フィネレノンの血中濃度が上昇し作用が増強するおそれがある(本剤はフィネレノンの代謝酵素(CYP3A4)を阻害する)]。
22). エプレレノン<セララ>〔2.1参照〕[本剤との併用により、エプレレノンの血中濃度が上昇し作用が増強するおそれがある(本剤はエプレレノンの代謝酵素(CYP3A4)を阻害する)]。
23). ボクロスポリン<ルプキネス>〔2.1参照〕[本剤との併用により、ボクロスポリンの血中濃度が上昇し作用が増強するおそれがある(本剤はボクロスポリンの代謝酵素(CYP3A4)を阻害する)]。
24). マバカムテン<カムザイオス>〔2.1参照〕[本剤との併用により、マバカムテンの血中濃度が上昇し副作用が増強され収縮機能障害による心不全のリスクが高まるおそれがある(本剤はマバカムテンの代謝酵素(CYP3A4)を阻害する)]。
10.2. 併用注意:
1). ベネトクラクス(再発又は難治性の慢性リンパ性白血病(小リンパ球性リンパ腫を含む)の維持投与期、急性骨髄性白血病)[本剤との併用により、ベネトクラクスの血中濃度が増加するおそれがあるので、ベネトクラクスを減量するとともに、患者の状態を慎重に観察し、副作用の発現に十分注意すること(本剤はベネトクラクスの代謝酵素(CYP3A)を阻害する)]。
2). バレメトスタット[本剤との併用により、バレメトスタットの血中濃度が増加するおそれがあるので、バレメトスタットを減量するとともに、患者の状態を慎重に観察し、副作用の発現に十分注意すること(本剤はバレメトスタットの代謝酵素(CYP3A)を阻害する)]。
3). 抗てんかん薬:
①. 抗てんかん薬(フェニトイン)[フェニトインとの併用により、本剤のCmaxは49%・AUCは69%減少した(フェニトインは、本剤の代謝酵素(CYP3A4)を誘導する)]。
②. 抗てんかん薬(フェニトイン)[本剤との併用により、フェニトインのCmaxは1.7倍・AUCは1.8倍増加した(本剤はフェニトインの代謝酵素(CYP2C9)を阻害する)]。
4). レテルモビル[レテルモビルとの併用により、本剤のCmaxは39%・AUC0-12は44%減少し、レテルモビルとの併用により、作用が減弱するおそれがある(レテルモビルは本剤の代謝酵素(CYP2C19及びCYP2C9)を誘導すると考えられる)]。
5). チロシンキナーゼ阻害剤(ボスチニブ、ニロチニブ、イブルチニブ、ラロトレクチニブ、ロルラチニブ)[本剤との併用により、これらの薬剤の血中濃度が増加するおそれがあるため、代替薬への変更を考慮すること(本剤はこれらの薬剤の代謝酵素(CYP3A)を阻害する)]。
6). HIVプロテアーゼ阻害薬:
①. HIVプロテアーゼ阻害薬<リトナビルは禁忌>(ホスアンプレナビル)[本剤との併用により、ホスアンプレナビルの活性代謝物であるアンプレナビルの血中濃度が増加するおそれがある(In vitro試験結果において、本剤はアンプレナビルの代謝酵素(CYP3A4)を阻害した)]。
②. HIVプロテアーゼ阻害薬<リトナビルは禁忌>(ホスアンプレナビル)[ホスアンプレナビルとの併用により、本剤の血中濃度が増加するおそれがある(In vitro試験において、アンプレナビルは本剤の代謝酵素(CYP3A4)を阻害した)]。
7). 非ヌクレオシド逆転写酵素阻害薬(NNRTI):
①. 非ヌクレオシド逆転写酵素阻害薬
②. 非ヌクレオシド逆転写酵素阻害薬
③. 非ヌクレオシド逆転写酵素阻害薬
8). トレチノイン[本剤との併用により、トレチノインの血中濃度が増加するおそれがある(本剤はトレチノインの代謝酵素(CYP)を阻害する)]。
9). 免疫抑制剤:
①. 免疫抑制剤(シクロスポリン)[本剤との併用により、シクロスポリンのCmaxは1.1倍にAUCは1.7倍に増加した(本剤はこれらの薬剤の代謝酵素(CYP3A4)を阻害する)]。
②. 免疫抑制剤(タクロリムス)[本剤との併用により、タクロリムスのCmaxは2.2倍にAUCは3.2倍に増加した(本剤はこれらの薬剤の代謝酵素(CYP3A4)を阻害する)]。
③. 免疫抑制剤(エベロリムス)[本剤との併用により、エベロリムスの血中濃度が増加するおそれがある(本剤はこれらの薬剤の代謝酵素(CYP3A4)を阻害する)]。
10). クマリン系抗凝血薬(ワルファリンカリウム)〔8.8参照〕[本剤との併用により、プロトロンビン時間が1.9倍延長し、また、ワルファリンの作用が増強し著しいINR上昇を来した症例が報告されている(本剤はワルファリンの代謝酵素(CYP2C9)を阻害する)]。
11). プロトンポンプ阻害薬(オメプラゾール)[本剤との併用により、オメプラゾールのCmaxは2.2倍・AUCは3.8倍増加した(本剤はオメプラゾールの代謝酵素(CYP2C19及びCYP3A4)を阻害する)]。
12). ミダゾラム[本剤との併用により、ミダゾラム0.05mg/kg単回静脈内投与時のミダゾラムのAUCは3.7倍に増加(本剤はミダゾラムの代謝酵素(CYP3A4)を阻害する)し、ミダゾラム7.5mg単回経口投与(本邦未承認)時のミダゾラムのCmaxは3.8倍にAUCは10.3倍に増加した(本剤はミダゾラムの代謝酵素(CYP3A4)を阻害する)]。
13). HMG-CoA還元酵素阻害薬[本剤との併用により、HMG-CoA還元酵素阻害薬の血中濃度が増加するおそれがある(In vitro試験において、本剤はHMG-CoA還元酵素阻害薬の代謝酵素(CYP3A4)を阻害した)]。
14). ジアゼパム[本剤との併用により、ジアゼパムのAUCは増加し血中濃度半減期は延長した(本剤はジアゼパムの代謝酵素(CYP3A4及びCYP2C19)を阻害する)]。
15). ゾルピデム[本剤との併用により、ゾルピデムのCmaxは1.2倍・AUCは1.5倍増加した(本剤はゾルピデムの代謝酵素(CYP3A4及びCYP2C9)を阻害する)]。
16). スルホニル尿素系血糖降下薬(トルブタミド)[本剤との併用により、これらの薬剤の血中濃度が増加するおそれがある(本剤はこれらの薬剤の代謝酵素(CYP2C9)を阻害する)]。
17). ビンカアルカロイド系抗悪性腫瘍薬(ビンクリスチン、ビンブラスチン)[本剤との併用により、これらの薬剤の血中濃度が増加するおそれがある(本剤はこれらの薬剤の代謝酵素(CYP3A4)を阻害する)]。
18). メサドン[本剤との併用により、メサドンのCmaxが30.7%・AUCが47.2%増加した(本剤はこれらの薬剤の代謝酵素(CYP3A4)を阻害する)]。
19). オキシコドン[本剤との併用により、オキシコドンのCmaxとAUCが増加した(本剤はこれらの薬剤の代謝酵素(CYP3A4)を阻害する)]。
20). フェンタニル[本剤との併用により、フェンタニルのAUCが増加した(本剤はこれらの薬剤の代謝酵素(CYP3A4)を阻害する)]。
21). イブプロフェン、ジクロフェナク[本剤との併用により、これらの薬剤のCmaxとAUCが増加した(本剤はこれらの薬剤の代謝酵素(CYP2C9)を阻害する)]。
22). 経口避妊薬:
①. 経口避妊薬(ノルエチステロン・エチニルエストラジオール)[ノルエチステロン・エチニルエストラジオールとの併用により、本剤のCmaxは14%・AUCは46%増加した(これらの薬剤は本剤の代謝酵素(CYP2C19)を阻害する)]。
②. 経口避妊薬(ノルエチステロン・エチニルエストラジオール)[本剤との併用により、エチニルエストラジオールのCmaxは36%・AUCは61%増加し、ノルエチステロンのCmaxは15%・AUCは53%増加した(本剤はこれらの薬剤の代謝酵素(CYP3A4)を阻害する)]。
23). リオシグアト[本剤との併用により、リオシグアトの血中濃度が上昇するおそれがあるので、本剤との併用が必要な場合は、患者の状態に注意し、必要に応じてリオシグアトの減量を考慮すること(本剤はリオシグアトの代謝酵素(CYP3A)を阻害する)]。
24). セイヨウオトギリソウ<セント・ジョーンズ・ワート>含有食品(St.John’s Wort)[セイヨウオトギリソウとの併用により、本剤のAUCは59%減少したので、本剤投与時はセイヨウオトギリソウ含有食品を摂取しないよう注意すること(セイヨウオトギリソウは、本剤の代謝酵素(CYP3A4)を誘導する)]。
(その他の注意)
15.1. 臨床使用に基づく情報
15.1.1. 外国人患者において、ボリコナゾールの血漿中濃度と肝機能検査値異常発現率の間に統計的に有意な関連性が認められた。日本人健康成人においては、肝機能障害が発生した症例で、かつ、血漿中濃度が測定されていた症例の血漿中濃度トラフ値はいずれも4.5μg/mL以上であった。また、国内臨床試験では有効性及び安全性に応じた投与量の調整に加え、目安としてトラフ血漿中濃度が4.5μg/mL以上の場合、必要に応じて投与量を減量する血中濃度モニタリングを実施した。国内外の臨床試験データからは肝機能検査値異常の出現を予測する血漿中濃度の閾値は認められていない〔7.4、8.7参照〕。
15.1.2. 肺移植あるいは心肺移植患者を対象とした海外の観察研究において、本剤曝露患者では皮膚扁平上皮癌の発生リスクがアゾール系抗真菌薬非曝露患者と比較して有意に高く(ハザード比:2.39、95%信頼区間1.31-4.37)、この発生リスクは180日を超える長期曝露の患者で高い(ハザード比:3.52、95%信頼区間1.59-7.79)との報告がある。
15.1.3. 本剤投与後に、皮膚扁平上皮癌及び悪性黒色腫が発生したとの報告がある。また、本剤長期投与中に、光線過敏性反応を発現している患者で皮膚扁平上皮癌及び悪性黒色腫が発生したとの報告がある〔8.6参照〕。
(取扱い上の注意)
開封後は、湿気を避けて保存すること。
(保管上の注意)
室温保存。
副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1. 重大な副作用
11.1.1. ショック(頻度不明)、アナフィラキシー(頻度不明)。
11.1.2. 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(頻度不明)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明)、多形紅斑(頻度不明):皮疹等の症状があらわれた場合には投与を中止し、適切な処置を行うこと。
11.1.3. 肝障害(5.0%):重篤な肝障害(肝炎、黄疸、肝不全、肝性昏睡等)があらわれることがあり、死亡例も報告されている〔1.2、8.2参照〕。
11.1.4. 心電図QT延長(頻度不明)、心室頻拍(1.0%)、心室細動(頻度不明)、不整脈(頻度不明)、完全房室ブロック(頻度不明):心電図QT延長、心室頻拍(torsade de pointesを含む)、心室細動、不整脈、完全房室ブロック、心室性二段脈、心室性期外収縮、頻脈等があらわれることがある〔8.3、9.1.2参照〕。
11.1.5. 心不全(3.0%):心機能に関する異常が認められた場合には投与を中止し、適切な処置を行うこと。
11.1.6. 腎障害(1.0%):重篤な腎障害(急性腎障害、腎炎、腎尿細管壊死等)があらわれることがある〔8.1参照〕。
11.1.7. 呼吸窮迫症候群(頻度不明)。
11.1.8. ギラン・バレー症候群(頻度不明)。
11.1.9. 血液障害(2.0%):骨髄抑制、汎血球減少、再生不良性貧血、無顆粒球症、播種性血管内凝固等の重篤な血液障害があらわれることがある〔8.1参照〕。
11.1.10. 偽膜性大腸炎(頻度不明):偽膜性大腸炎等の重篤な大腸炎があらわれることがあるので、腹痛、下痢があらわれた場合には投与を中止し、適切な処置を行うこと。
11.1.11. 痙攣(頻度不明):痙攣等の神経障害があらわれることがある。
11.1.12. 横紋筋融解症(頻度不明):筋肉痛、脱力感、CK上昇、血中ミオグロビン上昇及び尿中ミオグロビン上昇を特徴とする横紋筋融解症があらわれることがある。
11.1.13. 間質性肺炎(0.2%*):咳嗽、呼吸困難、発熱、肺音異常(捻髪音)等が認められた場合には、速やかに胸部X線、速やかに胸部CT、速やかに血清マーカー等の検査を実施し、本剤の投与を中止するとともに、副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.1.14. 低血糖(頻度不明):重篤な低血糖があらわれることがある。
11.1.15. 意識障害(0.1%*):意識消失、意識レベル低下等の意識障害があらわれることがある。
11.1.16. 高カリウム血症(1.0%)〔8.1参照〕。
*:発現頻度は使用成績調査の結果に基づいている。
11.2. その他の副作用
1). 血液及びリンパ系障害:(1~5%未満)白血球減少症、血小板減少症、(頻度不明)貧血、リンパ節症。
2). 心臓障害:(1~5%未満)動悸、心嚢液貯留、(頻度不明)肺水腫、脚ブロック。
3). 耳・迷路障害:(1~5%未満)聴覚過敏、耳鳴、回転性眩暈。
4). 内分泌障害:(1~5%未満)ADH不適合分泌、(頻度不明)副腎皮質機能不全、甲状腺機能亢進症、甲状腺機能低下症。
5). 眼障害:(5%以上)※羞明、※霧視、※視覚障害、(1~5%未満)眼異常感、眼調節障害、色覚異常、複視、眼瞼浮腫、流涙増加、縮瞳、視神経乳頭浮腫、光視症、網膜滲出物、網膜出血、網膜毛細血管瘤、網膜裂孔、網膜血管炎、黄視症、(頻度不明)眼瞼炎、視神経炎、強膜炎、角膜混濁、視神経萎縮。
6). 胃腸障害:(5%以上)悪心、嘔吐、(1~5%未満)腹部膨満、口唇ひび割れ、便秘、下痢、消化不良、胃潰瘍、痔核、イレウス、口唇乾燥、口唇粘膜脱落、口唇炎、逆流性食道炎、口内炎、(頻度不明)腹痛、胃腸炎、十二指腸炎、歯肉炎、舌炎、膵炎、舌浮腫、腹膜炎。
7). 全身障害及び投与局所様態:(1~5%未満)無力症、胸痛、胸部圧迫感、異常感、倦怠感、末梢性浮腫、発熱、口渇、(頻度不明)悪寒、注射部位反応/注射部位炎症、インフルエンザ症候群。
8). 肝胆道系障害:(頻度不明)胆嚢炎、胆石症、肝腫大。
9). 感染症及び寄生虫症:(頻度不明)副鼻腔炎。
10). 代謝及び栄養障害:(5%以上)食欲不振、(1~5%未満)高血糖、低カリウム血症、(1%未満*)低ナトリウム血症、(頻度不明)高コレステロール血症。
11). 筋骨格及び結合組織障害:(1~5%未満)背部痛、四肢痛、(1%未満*)関節炎、(頻度不明)骨膜炎。
12). 神経系障害:(5%以上)頭痛、(1~5%未満)認知不能症、健忘、浮動性めまい、味覚異常、感覚減退、傾眠、会話障害、振戦、視野欠損、(1%未満*)末梢性ニューロパチー、(頻度不明)錯感覚、失調、脳浮腫、筋緊張亢進、眼振、失神、注視痙攣、錐体外路症候群。
13). 精神障害:(5%以上)不眠症、(1~5%未満)錯乱状態、幻覚、幻聴、幻視、(1%未満*)不安、(頻度不明)うつ病、激越。
14). 腎及び尿路障害:(頻度不明)血尿、アルブミン尿。
15). 呼吸器、気管支及び縦隔障害:(1~5%未満)喀血。
16). 皮膚及び皮下組織障害:(1~5%未満)皮膚乾燥、湿疹、紅斑、結節性紅斑、発疹、毛髪変色、光線過敏性反応、多汗、皮膚そう痒症、丘疹、皮膚落屑、(1%未満*)蕁麻疹、(頻度不明)顔面浮腫、斑状丘疹状皮疹、脱毛症、剥脱性皮膚炎、紫斑、固定薬疹、乾癬、血管浮腫、皮膚エリテマトーデス、偽性ポルフィリン症。
17). 血管障害:(1~5%未満)潮紅、(頻度不明)低血圧、血栓性静脈炎、静脈炎、リンパ管炎。
18). 臨床検査:(5%以上)ALT増加、AST増加、ALP増加、γ-GTP増加、(1~5%未満)血中ビリルビン増加、血中カルシウム増加、血中クレアチニン増加、LDH増加、血中カリウム減少、血中カリウム増加、血圧低下、血圧上昇、フィブリンDダイマー増加、血清FDP増加、膵アミラーゼ増加、好酸球増加、血小板数減少、(1%未満*)BUN増加。
発現頻度は重症又は難治性真菌感染症の承認時の国内臨床試験の結果に基づいている。
*:発現頻度は使用成績調査の結果に基づいている。
※:〔1.3、8.5参照〕。
薬物動態
16.1 血中濃度
16.1.1 単回投与
日本人健康成人男性(各用量6例)に、ボリコナゾール100、200、300及び400mgを空腹時に単回経口投与したとき、消失半減期は用量に依存して延長し、AUC及びCmaxは用量に対して非線形の増加を示した。
表16-1 薬物動態パラメータ
<<表省略>>
16.1.2 反復投与
(1)健康成人
ボリコナゾールは、主にCYP2C19により代謝される。CYP2C19には遺伝子多型が存在するため、遺伝子のタイプにより標準的(EM:Extensive Metabolizer)、やや低い(HEM:Heterozygous Extensive Metabolizer)及び低い(PM:Poor Metabolizer)酵素活性を有する被験者に分けて解析した。
日本人健康成人男性に、ボリコナゾール1回200mgを1日2回反復経口投与(負荷投与:初日に1回400mgを1日2回)したところ、EM及びHEMで2日目、PMで3日目にほぼ定常状態に達した。
表16-2 投与7日目の薬物動態パラメータ
<<表省略>>
(2)小児患者
日本人小児患者(3~14歳、18例)にボリコナゾール1回8mg/kgを1日2回(負荷投与:初日に1回9mg/kgを1日2回)7日間静脈内投与した後、ドライシロップとして1回9mg/kgを1日2回7日間反復経口投与したときの最終投与後のCmax及びAUCτの幾何平均値(範囲)はそれぞれ7.22(2.03~18.3)μg/mL及び45.8(10.0~156)μg・h/mLであった。[7.2参照]
表16-3 投与7日目の薬物動態パラメータ
<<表省略>>
16.1.3 生物学的同等性試験
ボリコナゾール顆粒20%「タカタ」とブイフェンド錠200mgを、クロスオーバー法によりそれぞれ1g又は1錠(ボリコナゾールとして200mg)健康成人男子(CYP2C19のPMを除く)に絶食単回経口投与して血漿中未変化体濃度を測定し、得られた薬物動態パラメータ(AUC、Cmax)について90%信頼区間法にて統計解析を行った結果、log(0.80)~log(1.25)の範囲であり、両剤の生物学的同等性が確認された。
図16-1 血漿中濃度
<<図省略>>
表16-4 薬物動態パラメータ
<<表省略>>
血漿中濃度並びにAUC、Cmax等のパラメータは、被験者の選択、体液の採取回数・時間等の試験条件によって異なる可能性がある。
16.2 吸収
16.2.1 バイオアベイラビリティ
ポピュレーションファーマコキネティクス解析から、日本人及び外国人における健康成人のボリコナゾールのバイオアベイラビリティは96%と推定された。国内臨床第III相試験における患者のバイオアベイラビリティは、ほぼ100%であった。
16.2.2 食事の影響
健康成人男性(37例)において、高脂肪食(約1000kcal)を取った直後にボリコナゾール200mgを1日2回(負荷投与:初日に1回400mgを1日2回)7日間反復経口投与したとき、定常状態におけるCmax及びAUCτは空腹時投与と比較し、それぞれ34%及び24%低下した。Tmaxは食事により1.4時間遅延した(外国人データ)。
16.3 分布
健康成人のボリコナゾールの定常状態における分布容積は4.6L/kgと推定された(日本人及び外国人データ)。
16.3.1 組織内移行
ボリコナゾール投与後1~10時間の血漿中ボリコナゾール濃度に対する髄液中ボリコナゾール濃度の比は0.22~1.0(中央値0.46)であった(外国人データ)。
16.3.2 蛋白結合率
ボリコナゾールのヒト血漿蛋白に対する結合率は、58%であった。
16.4 代謝
In vitro試験において、ボリコナゾールはCYP2C19、CYP2C9及びCYP3A4によって代謝される。ボリコナゾールの主要代謝物はN-オキシドである。[8.9、10.参照]
16.5 排泄
ボリコナゾールは、肝代謝により消失し、単回投与後96時間までに尿中に未変化体として投与量の2%未満が排泄される。
16.6 特定の背景を有する患者
16.6.1 肝機能の低下した被験者
健康成人にボリコナゾール1回200mgを1日2回(負荷投与1回400mgを1日2回)及び中等度の肝機能低下者(Child-Pugh分類クラスB)にボリコナゾール1回100mgを1日2回(負荷投与1回200mgを1日2回)反復経口投与したときの最終投与後のAUCτは両群で同じであった。このとき血漿中ボリコナゾール濃度は、健康成人では投与2日目にはほぼ定常状態に達したが、中等度肝機能低下者では6日目まで定常状態に達しなかった(外国人データ)。[7.4、9.3.2参照]
16.6.2 腎機能の低下した被験者
(1)中等度の腎機能低下患者(クレアチニンクリアランス30~50mL/min)
ボリコナゾール1回3mg/kgを1日2回(負荷投与1回6mg/kgを1日2回)7日間反復静脈内投与したとき、腎機能が正常な被験者と比べAUC及びCmaxに有意差は認められなかった(外国人データ)。
(2)血液透析
4時間の血液透析により血漿中ボリコナゾールの8%が除去された(外国人データ)。
臨床成績
17.1 有効性及び安全性に関する試験
〈重症又は難治性真菌感染症〉
17.1.1 国内第III相試験(1501001試験)
深在性真菌症と診断された患者又は深在性真菌症が強く疑われた患者を対象とし、100例(経口療法61例、静注療法18例、スイッチ療法21例)にボリコナゾールを投与した。
経口療法の場合は、投与初日に負荷用量として300mgを1日2回(体重40kg未満の場合は150mgを1日2回)、その後は維持用量として200mgを1日2回(体重40kg未満の場合は100mgを1日2回)経口投与した。ただし、投与開始3日目の血漿中ボリコナゾール濃度が2.5μg/mL以上のときは、投与開始5日目以降は150mgを1日2回経口投与へ減量した。
静注療法の場合は、重篤な真菌症の場合は、投与初日に負荷用量として6mg/kgを1日2回、その後は維持用量として4mg/kgを1日2回静脈内投与した。ただし、投与開始3日目の血漿中ボリコナゾール濃度が2.5μg/mL以上のときは、投与開始5日目以降は3mg/kgを1日2回静脈内投与に減量した。重篤な真菌症以外の場合は、投与初日に負荷用量として6mg/kgを1日2回、その後は維持用量として3mg/kgを1日2回静脈内投与した。静注療法を3日間行った後、治験責任医師により経口療法が可能と判断された患者においては経口療法への切り替え(スイッチ療法)を可能とし、投与開始3日目の血漿中濃度が2.5μg/mL未満のときは200mgを1日2回、2.5μg/mL以上のときは150mgを1日2回経口投与した。
投与終了時(最大投与期間12週間)の総合効果有効率は、次の通りであった。
表17-1 投与終了時(最大投与期間12週間)の総合効果有効率
<<表省略>>
副作用発現率(臨床検査値異常を含む)は、総症例100例中78例(78.0%)であった。主な副作用は、羞明(25.0%)、視覚障害(24.0%)、肝機能検査値異常(13.0%)、悪心(8.0%)、嘔吐(8.0%)、頭痛(8.0%)、γ-GTP増加(7.0%)、肝障害(6.0%)、ALP増加(5.0%)、霧視(5.0%)、食欲不振(5.0%)等であった。
17.1.2 外国第III相試験(150-307/602試験)
免疫不全で急性侵襲性アスペルギルス症の患者を対象とし、ボリコナゾール投与群とアムホテリシンB投与群の有効性、安全性及び忍容性を比較した。ボリコナゾール投与群では196例に初回投与24時間は負荷用量として6mg/kgを12時間ごとに、以降は4mg/kgを12時間ごとに静脈内投与した。忍容性に問題が認められた場合は3mg/kgを12時間ごとへの減量を可能とした。全ての被験者に対して、少なくとも7日間の静脈内投与を推奨し、注入速度は最大で3mg/kg/hとした。ボリコナゾールの経口投与の開始用量は200mgを1日2回とし、経口投与3日目以降に臨床効果が不十分な場合は、300mgを1日2回までの増量を可能とした。忍容性に問題が認められた場合は50mgを1日2回単位の減量を行い、200mgを1日2回までの減量を可能とした。体重40kg未満の被験者においては、ボリコナゾールの経口投与量を半量とした。
投与終了時(最大投与期間16週間)の総合効果有効率は、次の通りであった。
表17-2 投与終了時(最大投与期間16週間)の総合効果有効率
<<表省略>>
副作用発現率は196例中128例(65.3%)であった。主な副作用は、視覚異常(28.1%)、嘔気(7.1%)、発疹(6.6%)であった。
17.1.3 外国第III相試験(150-309/604試験)
「原因真菌に対して効能を有する薬剤がない全身性又は侵襲性真菌症」、又は「前治療薬が効能不十分又は忍容性の問題から継続できない全身性又は侵襲性真菌症」と診断された患者を対象に、372例にボリコナゾールを静脈内投与又は経口投与した。
静脈内投与の場合は、投与初日に負荷用量として6mg/kgを12時間ごとに投与し、その後は維持用量として4mg/kgを12時間ごとに少なくとも3日間投与した。注入速度は約3mg/kg/hとした。経口投与の場合は、投与初日に負荷用量として400mgを1日2回投与し、その後は維持用量として200mgを1日2回投与した。
投与終了時(最大投与期間16週間)の総合効果有効率は、次の通りであった。
表17-3 投与終了時(最大投与期間16週間)の総合効果有効率
<<表省略>>
副作用発現率は372例中215例(57.8%)であった。主な副作用は、視覚異常(22.8%)、発疹(7.5%)、嘔気(6.5%)であった。
17.1.4 外国第III相試験(150-608試験)
非好中球減少のカンジダ血症患者を対象に、ボリコナゾールの有効性及び安全性を、アムホテリシンBの投与後にフルコナゾールを投与した時の有効性及び安全性と比較した。少なくとも最初の3日間は静脈内投与を行い、その後は経口投与への切り替えを可能とした。
ボリコナゾール投与群では272例に最初の24時間は負荷用量として6mg/kgを、以後は維持用量として3mg/kgをそれぞれ12時間ごとに静脈内投与した。また、維持用量は4mg/kgを12時間ごとまで増量できることとした。最高注入速度は3mg/kg/hとした。
ボリコナゾール経口投与への切り替え後は、200mgを1日2回(体重40kg未満の場合は100mgを1日2回)で開始し、300mgを1日2回(体重40kg未満の場合は150mgを1日2回)まで増量可能とした。
投与終了時(最大投与期間はカンジダ血症の消失後8週間)の総合効果有効率は次の通りであった。
表17-4 投与終了時(最大投与期間はカンジダ血症の消失後8週間)の総合効果有効率
<<表省略>>
副作用発現率は272例中97例(35.7%)であった。主な副作用はALP増加(0.7%)、低カリウム血症(0.7%)であった。
〈造血幹細胞移植患者における深在性真菌症の予防〉
17.1.5 海外第III相試験(無作為化非盲検並行群間比較試験)(A1501073試験)
過去6ヵ月間に侵襲性真菌感染症の発症がない12歳以上の造血幹細胞移植患者を対象として、移植後180日の真菌感染予防の成功についてボリコナゾールとイトラコナゾールを比較した。ボリコナゾール又はイトラコナゾールを2日間静脈内投与し、その後は経口投与に切り替えた。ボリコナゾール投与群では234例に、最初の24時間は負荷用量として6mg/kgを、以後は維持用量として4mg/kgをそれぞれ12時間ごとに静脈内投与した。経口投与に切り替え後は、200mgを1日2回(体重40kg未満の場合は100mgを1日2回)投与した。
イトラコナゾール投与群では255例に、負荷用量として200mgを1日2回静脈内投与し、経口投与へ切り替え後は200mgを1日2回投与した。
移植後180日における真菌感染予防の成功率は、次の通りであった。
表17-5 移植後180日における真菌感染予防の成功率
<<表省略>>
ボリコナゾール投与群における副作用発現率は233例中123例(52.8%)であった。主な副作用は、悪心(7.7%)、肝毒性(7.3%)、視力障害(6.0%)及び肝機能検査異常(5.2%)であった。
17.1.6 海外第III相試験(非盲検非対照試験)(A1501038試験)
過去12ヵ月間に侵襲性真菌感染症の既往のある18歳以上の造血幹細胞移植患者を対象として、侵襲性真菌感染症の二次予防のために45例にボリコナゾールを投与した。静脈内投与では、負荷投与として12時間ごとに6mg/kgを2回投与し、維持投与として12時間ごとに4mg/kgを投与した。経口投与では、負荷投与として12時間ごとに400mgを2回投与(体重40kg未満の場合は12時間ごとに200mgを2回投与)し、維持投与として12時間ごとに200mg(体重40kg未満の場合は12時間ごとに100mg)を投与した。投与開始12ヵ月後までに侵襲性真菌感染症を発症した被験者の割合は10.7%(3/28例)であった。
副作用発現率は45例中26例(57.8%)であった。主な副作用は、肝毒性(8.9%)、幻覚(6.7%)及び頭痛(6.7%)であった。
薬効薬理
18.1 作用機序
ボリコナゾールは真菌細胞において、膜成分のエルゴステロール生合成を阻害することにより抗真菌作用を示す。また、ボリコナゾールのエルゴステロール生合成阻害作用は真菌に選択的で、ラット肝細胞でのステロール生合成に対する影響は少ない。
18.2 抗真菌作用
18.2.1 ボリコナゾールは、カンジダ属、アスペルギルス属、クリプトコックス属、フサリウム属及びスケドスポリウム属に対しin vitroで抗真菌活性を示した。
18.2.2 ボリコナゾールは、アスペルギルス属に対して殺菌作用を示した。
18.2.3 免疫正常及び免疫抑制モルモットの実験的カンジダ症、クリプトコックス症、アスペルギルス症及びスケドスポリウム症に対して高い感染防御効果を示した。
医師の処方により使用する医薬品。



 で医薬品を比較する
で医薬品を比較する
