メソトレキセート錠2.5mg
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
特定薬剤管理指導加算等の
算定対象となる薬剤
医薬品コード(YJコード):4222001F1027
- 収載区分
- 銘柄別収載
- 先発・後発情報
- その他
- オーソライズド
ジェネリック - -
- 一般名
- メトトレキサート錠
- 英名(商品名)
- Methotrexate
- 規格
- 2.5mg1錠
- 薬価
- 18.50
- メーカー名
- ファイザー
- 規制区分
- 劇薬
- 長期投与制限
- -
- 標榜薬効
- 抗悪性腫瘍薬〔代謝拮抗薬〕
- 色
- 淡黄褐
- 識別コード
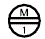
- (本体)@ (本体)LL (本体)M 1
- [@: メーカーロゴ]
- 添付文書
-
PDF 2026年3月改訂(第2版)
- 告示日
- -
- 経過措置期限
- -
- 医薬品マスタに反映
- -
- 医薬品マスタ削除予定
- -
- 運転注意
- 情報なし(使用の適否を判断するものではありません)
- ドーピング
- 禁止物質なし(使用の適否を判断するものではありません)
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
外形画像


改訂情報
2026年3月31日 DSU No.344 【その他】
【8.重要な基本的注意】(追記)
光線過敏症が報告されているので、適切な日焼け防止対策を行い、強い日光又は紫外線への曝露を避けるよう患者に指導すること。
【10.2併用注意】(一部改訂)
効能効果
次記疾患の自覚的並びに他覚的症状の緩解:1)急性白血病、2)絨毛性疾患(絨毛癌、破壊胞状奇胎、胞状奇胎)、3)慢性リンパ性白血病、4)慢性骨髄性白血病。
用法用量
〈白血病〉
メトトレキサートとして、通常、次の量を1日量として1週間に3~6日経口投与する。
幼児1.25~2.5mg。
小児2.5~5mg。
成人5~10mg。
〈絨毛性疾患〉
1クールを5日間とし、メトトレキサートとして、通常、成人1日10~30mgを経口投与する。休薬期間は、通常、7~12日間であるが、前回の投与によって副作用があらわれた場合は、副作用が消失するまで休薬する。
なお、いずれの場合でも年齢、症状により適宜増減する。
警告・禁忌・相互作用・その他の注意
(禁忌)
2.1. 本剤の成分に対し重篤な過敏症の既往歴のある患者。
2.2. 肝障害のある患者〔9.3肝機能障害患者の項参照〕。
2.3. 腎障害のある患者〔9.2腎機能障害患者の項参照〕。
2.4. 胸水、腹水等のある患者[胸水、腹水等に長時間貯留して毒性が増強されることがある]。
(重要な基本的注意)
8.1. 骨髄機能抑制、肝機能障害・腎機能障害等の重篤な副作用が起こることがあるので、頻回に臨床検査(血液検査、肝機能・腎機能検査、尿検査等)を行うなど、患者の状態を十分観察すること。また、使用が長期間にわたると副作用が強くあらわれ、遷延性に推移することがあるので、投与は慎重に行うこと〔11.1.2、11.1.4、11.1.5参照〕。
8.2. 出血性腸炎、消化管潰瘍・消化管出血等の消化管障害があらわれることがあるので、口内炎、激しい腹痛、嘔吐、下痢等の症状があらわれた場合には投与を中止し、適切な処置を行うこと。また、患者に対し、口内炎があらわれた場合には、直ちに連絡するよう注意を与えること〔11.1.8参照〕。
8.3. 感染症の発現又は感染症増悪、出血傾向の発現又は出血傾向増悪に十分注意すること。また、患者に対し発熱、倦怠感があらわれた場合には、直ちに連絡するよう注意を与えること〔11.1.3参照〕。
8.4. 免疫機能が抑制された患者への生ワクチン接種により、ワクチン由来の感染を増強又は持続させるおそれがあるので、本剤投与中に生ワクチンを接種しないこと。
8.5. 本剤投与に先立って、肝炎ウイルス感染の有無を確認すること〔9.1.4、11.1.4参照〕。
8.6. 光線過敏症が報告されているので、適切な日焼け防止対策を行い、強い日光又は紫外線への曝露を避けるよう患者に指導すること〔10.2参照〕。
(特定の背景を有する患者に関する注意)
(合併症・既往歴等のある患者)
9.1.1. 骨髄機能抑制のある患者:骨髄機能抑制を増悪させるおそれがある〔11.1.2参照〕。
9.1.2. 感染症を合併している患者:骨髄機能抑制により感染を増悪させるおそれがある〔11.1.3参照〕。
9.1.3. 水痘患者:致命的全身障害があらわれることがある。
9.1.4. B型又はC型肝炎ウイルスキャリアの患者:B型肝炎ウイルスキャリアの患者及びB型肝炎既往感染者(HBs抗原陰性かつHBc抗体陽性又はHBs抗原陰性かつHBs抗体陽性)又はC型肝炎ウイルスキャリアの患者に対し本剤を投与する場合、投与期間中及び投与終了後は継続して肝機能検査や肝炎ウイルスマーカーのモニタリングを行うなど、B型又はC型肝炎ウイルス増殖の徴候や症状の発現に注意すること(重篤な肝炎や肝障害の発現が報告されており、死亡例が認められている。またB型肝炎ウイルスキャリアの患者の場合、本剤投与終了後にB型肝炎ウイルスが活性化することによる肝炎等の発現も報告されている)〔8.5、11.1.4参照〕。
(腎機能障害患者)
腎機能障害患者:投与しないこと(本剤の排泄遅延により副作用が強くあらわれるおそれがある)〔2.3参照〕。
(肝機能障害患者)
肝機能障害患者:投与しないこと(肝障害を増悪させるおそれがある)〔2.2参照〕。
(生殖能を有する者)
小児及び生殖可能な年齢の患者に投与する必要がある場合には、性腺に対する影響を考慮すること〔9.7小児等の項参照〕。
(妊婦)
妊婦又は妊娠している可能性のある女性には投与しないことが望ましい(催奇形性を疑う症例報告があり、また、動物実験(マウス、ラット及びウサギ)で催奇形作用が報告されている)。
(授乳婦)
授乳しないことが望ましい(母乳中への移行が報告されている)。
(小児等)
副作用の発現に特に注意し、慎重に投与すること。低出生体重児、新生児、乳児<1歳未満>に対する臨床試験は実施していない〔9.4生殖能を有する者の項参照〕。
(高齢者)
腎機能検査値に十分注意し、患者の状態を観察しながら副作用の発現に特に注意し、慎重に投与すること(腎機能等生理機能が低下していることが多く、メトトレキサートの排泄遅延により副作用があらわれやすい)。
(相互作用)
10.2. 併用注意:
1). サリチル酸等の非ステロイド性抗炎症剤[メトトレキサートの副作用<骨髄抑制・肝・腎・消化管障害等>が増強されることがあるので、頻回に臨床検査を行うなど観察を十分に行い、異常が認められた場合には、メトトレキサートの減量、休薬等適切な処置を行い、また、メトトレキサートの拮抗剤であるホリナートカルシウム(ロイコボリンカルシウム)を投与すること(主として、非ステロイド性抗炎症剤の腎におけるプロスタグランジン合成阻害作用による腎血流量の低下及びナトリウム、水分貯留傾向のためメトトレキサートの排泄が遅延するためと考えられている)]。
2). スルホンアミド系薬剤、テトラサイクリン、クロラムフェニコール、フェニトイン、バルビツール酸誘導体[メトトレキサートの副作用<骨髄抑制・肝・腎・消化管障害・血液障害等>増強されることがあるので、頻回に臨床検査を行うなど観察を十分に行い、異常が認められた場合には、メトトレキサートの減量、休薬等適切な処置を行い、また、メトトレキサートの拮抗剤であるホリナートカルシウム(ロイコボリンカルシウム)を投与すること(併用薬剤が血漿蛋白と結合しているメトトレキサートを競合的に置換遊離し、メトトレキサートの濃度を上昇させ、その毒性を増強させる)]。
3). スルファメトキサゾール・トリメトプリム[メトトレキサートの副作用<骨髄抑制・肝・腎・消化管障害・血液障害等>増強されることがあるので、頻回に臨床検査を行うなど観察を十分に行い、異常が認められた場合には、メトトレキサートの減量、休薬等適切な処置を行い、また、メトトレキサートの拮抗剤であるホリナートカルシウム(ロイコボリンカルシウム)を投与すること(両薬剤の葉酸代謝阻害作用が協力的に作用するためと考えられている)]。
4). ペニシリン(ピペラシリン等)、プロベネシド[メトトレキサートの副作用<骨髄抑制・肝・腎・消化管障害・血液障害等>増強されることがあるので、頻回に臨床検査を行うなど観察を十分に行い、異常が認められた場合には、メトトレキサートの減量、休薬等適切な処置を行い、また、メトトレキサートの拮抗剤であるホリナートカルシウム(ロイコボリンカルシウム)を投与すること(併用薬剤がメトトレキサートの腎排泄を競合的に阻害するためと考えられている)]。
5). シプロフロキサシン[メトトレキサートの副作用<骨髄抑制・肝・腎・消化管障害・血液障害等>増強されることがあるので、頻回に臨床検査を行うなど観察を十分に行い、異常が認められた場合には、メトトレキサートの減量、休薬等適切な処置を行い、また、メトトレキサートの拮抗剤であるホリナートカルシウム(ロイコボリンカルシウム)を投与すること(発現機序の詳細は不明であるが、メトトレキサートの腎尿細管からの排泄が阻害されるためと考えられている)]。
6). レフルノミド[メトトレキサートの副作用<骨髄抑制・肝・腎・消化管障害・血液障害等>増強されることがあるので、頻回に臨床検査を行うなど観察を十分に行い、異常が認められた場合には、メトトレキサートの減量、休薬等適切な処置を行い、また、メトトレキサートの拮抗剤であるホリナートカルシウム(ロイコボリンカルシウム)を投与すること(併用により骨髄抑制等の副作用を増強するためと考えられている)]。
7). プロトンポンプ阻害剤(オメプラゾール、ラベプラゾール、ランソプラゾール等)[メトトレキサートの副作用<骨髄抑制・肝・腎・消化管障害・血液障害等>増強されることがあるので、頻回に臨床検査を行うなど観察を十分に行い、異常が認められた場合には、メトトレキサートの減量、休薬等適切な処置を行い、また、メトトレキサートの拮抗剤であるホリナートカルシウム(ロイコボリンカルシウム)を投与すること(機序は不明であるが、メトトレキサートの血中濃度が上昇することがある)]。
8). タラポルフィンナトリウム〔8.6参照〕[光線過敏症を起こすことがある(併用薬剤が光感受性を高めるため、光線過敏症を起こしやすい薬剤の作用を増強する)]。
9). 放射線療法[軟部組織壊死及び骨壊死の発現頻度が高まるという報告がある(機序不明)]。
(臨床検査結果に及ぼす影響)
トリメトプリム(スルファメトキサゾール・トリメトプリム配合剤)を併用した場合、DHFRを用いたメトトレキサート濃度の測定で見かけ上高値を呈することがあるので注意すること(DHFR
(過量投与)
13.1. 症状
外国で過量投与時に報告された主な症状は血液障害及び消化管障害であった(また、重篤な副作用を発現し、致命的経過をたどった症例が報告されている)。
13.2. 処置
過量投与したときは、すみやかに本剤の拮抗剤であるホリナートカルシウム(ロイコボリンカルシウム)を投与するとともに、本剤の排泄を促進するために水分補給と尿のアルカリ化を行うこと(本剤とホリナートカルシウムの投与間隔が長いほど、ホリナートカルシウムの効果が低下することがある)。
(その他の注意)
15.1. 臨床使用に基づく情報
15.1.1. 本剤を長期使用した患者あるいは本剤と他の抗悪性腫瘍剤を併用した患者に、悪性リンパ腫、急性白血病、骨髄異形成症候群(MDS)等の二次発癌が発生したとの報告がある。
15.1.2. 免疫機能が抑制された患者にワクチンを接種した場合、抗体反応の欠如が報告されている。
(取扱い上の注意)
瓶から取り出した錠剤は遮光して保存すること。
(保管上の注意)
室温保存。
副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。骨髄抑制、肝機能障害、粘膜障害・消化管障害等の細胞毒性に起因する副作用が発現した場合には、適切な処置を行いながら、本剤の拮抗剤であるホリナートカルシウム(ロイコボリンカルシウム)を投与すること。
11.1. 重大な副作用
11.1.1. ショック、アナフィラキシー(いずれも頻度不明):冷感、呼吸困難、血圧低下等があらわれることがある。
11.1.2. 骨髄抑制(頻度不明):汎血球減少、無顆粒球症(前駆症状として発熱、咽頭痛、インフルエンザ様症状等があらわれる場合がある)、白血球減少、血小板減少、貧血等の骨髄抑制、再生不良性貧血があらわれることがある〔8.1、9.1.1参照〕。
11.1.3. 感染症(頻度不明):呼吸不全にいたるような肺炎(ニューモシスティス肺炎等を含む)、敗血症、サイトメガロウイルス感染症、帯状疱疹等の重篤な感染症(日和見感染症を含む)があらわれることがあるので、患者の状態を十分観察し、異常が認められた場合には投与を中止し、抗生剤、抗菌剤の投与等の適切な処置を行うこと〔8.3、9.1.2参照〕。
11.1.4. 劇症肝炎、肝不全(いずれも頻度不明):劇症肝炎、肝不全、肝組織の壊死・肝組織の線維化、肝硬変等の重篤な肝障害(B型肝炎ウイルスによる肝障害又はC型肝炎ウイルスによる肝障害を含む)があらわれることがある〔8.1、8.5、9.1.4参照〕。
11.1.5. 急性腎障害、尿細管壊死、重症ネフロパチー(いずれも頻度不明):急性腎障害、尿細管壊死、重症ネフロパチー等の重篤な腎障害があらわれることがある〔8.1参照〕。
11.1.6. 間質性肺炎、肺線維症、胸水(いずれも頻度不明):間質性肺炎、肺線維症、胸水等があらわれ、呼吸不全にいたることがあるので、観察を十分に行い、発熱、咳嗽、呼吸困難等の呼吸器症状があらわれた場合には、速やかに胸部X線等の検査を行い、本剤の投与を中止するとともに副腎皮質ホルモン剤の投与等の適切な処置を行うこと。
11.1.7. 中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(いずれも頻度不明):発熱、紅斑、そう痒感、眼充血、口内炎等があらわれた場合には投与を中止し、適切な処置を行うこと。
11.1.8. 出血性腸炎、壊死性腸炎(いずれも頻度不明):出血性腸炎、壊死性腸炎等の重篤な腸炎があらわれることがあるので、激しい腹痛、下痢等の症状があらわれた場合には投与を中止し、適切な処置を行うこと〔8.2参照〕。
11.1.9. 膵炎(頻度不明)。
11.1.10. 骨粗鬆症(頻度不明):骨塩量減少等の異常が認められた場合には、投与を中止するなど適切な処置を行うこと。
11.1.11. 脳症(白質脳症を含む)(頻度不明)。
11.1.12. 進行性多巣性白質脳症(PML)(頻度不明):本剤投与中及び投与終了後は患者の状態を十分に観察し、意識障害、認知機能障害、麻痺症状(片麻痺、四肢麻痺)、構音障害、失語等の症状があらわれた場合は、MRIによる画像診断及び脳脊髄液検査を行うとともに、投与を中止し、適切な処置を行うこと。
11.2. その他の副作用
1). 過敏症:(頻度不明)発疹、蕁麻疹、そう痒、発熱。
2). 血液:(頻度不明)出血、低ガンマグロブリン血症、好酸球増多、リンパ節腫脹。
3). 肝臓:(頻度不明)黄疸、脂肪肝、AST上昇、ALT上昇、Al-P上昇、LDH上昇。
4). 腎臓:(頻度不明)血尿、BUN上昇、クレアチニン上昇、蛋白尿。
5). 消化器:(頻度不明)消化管潰瘍・消化管出血、口内炎、腹痛、下痢、食欲不振、嘔気・嘔吐、メレナ、イレウス、舌炎、口唇腫脹。
6). 皮膚:(頻度不明)光線過敏症、紅斑、皮膚色素沈着、皮膚色素脱出、皮下斑状出血、ざ瘡、脱毛、結節、皮膚潰瘍。
7). 精神神経系:(頻度不明)頭痛、眠気、目のかすみ、項部緊張、背部痛、しびれ感、味覚異常、意識障害、めまい、錯感覚。
8). 呼吸器:(頻度不明)咳嗽、呼吸困難。
9). 生殖器:(頻度不明)無精子症、卵巣機能不全、月経不全、流産。
10). その他:(頻度不明)膀胱炎、倦怠感、耳下腺炎、結膜炎、低蛋白血症、血清アルブミン減少、関節痛、動悸、胸部圧迫感、浮腫、悪寒。
メトトレキサート通常療法(本剤の効能又は効果、用法及び用量に基づく療法)においては、使用成績調査等の副作用発現頻度が明確となる調査を実施していない。
薬物動態
16.1 血中濃度
悪性腫瘍患者17例にメトトレキサートの2.25mg、4.50mg、9.00mg、31.5mgを経口単回投与したときの最高血中濃度は、2.25mg、4.50mg、9.00mg投与時には1時間後に、31.5mg投与時には2時間後にみられた。投与1時間後の最高血中濃度は5.3×10の-7乗mol/L~2.4×10の-6乗mol/Lであり、この濃度範囲内におけるメトトレキサートの血漿中蛋白結合率は約50%であった(外国人データ)。
16.5 排泄
悪性腫瘍患者17例にメトトレキサートの2.25mg、4.50mg、9.00mg、31.5mgを経口投与したときの尿中排泄率は24時間でほぼ100%を示した。
また、メトトレキサートの2.25~31.5mgを静脈内に投与したときの尿中排泄率は、最初の1時間で43%、6時間で88%であることが認められており、大部分は未変化体であった(外国人データ)。
薬効薬理
18.1 作用機序
メトトレキサートは、葉酸を核酸合成に必要な活性型葉酸に還元させる酵素dihydrofolate reductase(DHFR)の働きを阻止し、チミジル酸合成及びプリン合成系を阻害して、細胞増殖を抑制する。メトトレキサートは、正常細胞や感受性の高い癌細胞には能動的に取り込まれ、殺細胞作用を示す。
よく一緒に見られている薬
医師の処方により使用する医薬品。
特定薬剤管理指導加算等の算定対象となる薬剤。



 で医薬品を比較する
で医薬品を比較する
