アジンマ静注用1500
医療用
医療用医薬品:
医師の処方により使用する医薬品
医師の処方により使用する医薬品
医薬品コード(YJコード):3399418D1020
- 収載区分
- 銘柄別収載
- 先発・後発情報
- 先発品(後発品なし)
- オーソライズド
ジェネリック - -
- 一般名
- アパダムターゼ アルファ(遺伝子組換え)・シナキサダムターゼ アルファ(遺伝子組換え)注射用
- 英名(商品名)
- Adzynma
- 規格
- 1,500国際単位1瓶(溶解液付)
- 薬価
- 1,190,537.00
- メーカー名
- 武田薬品
- 規制区分
- -
- 長期投与制限
- -
- 標榜薬効
- 血小板凝集抑制薬〔von Willebrand因子切断酵素(ADAMTS13)製剤〕
- 色
- -
- 識別コード
- -
- [@: メーカーロゴ]
- 添付文書
-
PDF 2025年12月改訂(第4版)
- 告示日
- 2024年5月21日
- 経過措置期限
- -
- 医薬品マスタに反映
- 2024年6月版
- 医薬品マスタ削除予定
- -
- 運転注意
- 情報なし(使用の適否を判断するものではありません)
- ドーピング
- 禁止物質なし(使用の適否を判断するものではありません)
- CP換算
- -
- 長期収載品選定療養
- -
[識別コードの表記 @: メーカーロゴ]
改訂情報
2026年2月25日 DSU No.343 【その他】
【6.用法及び用量】(一部改訂)
本剤を添付の溶解液5mLで溶解し、2~4mL/分の速度で緩徐に静脈内に注射する。
定期的に投与する場合、通常、1回40国際単位/kgを隔週投与するが、患者の状態に応じて1回40国際単位/kgを週1回投与することができる。
急性増悪時に投与する場合、通常、1日目に1回40国際単位/kg、2日目に1回20国際単位/kg、3日目以降は1日1回15国際単位/kgを投与する。
【9.7小児等】(削除)
12歳未満の小児等を対象とした臨床試験は実施していない。
【11.2その他の副作用】(一部改訂)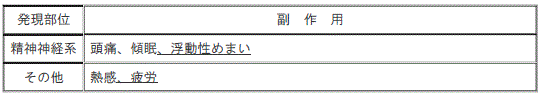
【11.2その他の副作用】(削除)
【15.1臨床使用に基づく情報】(一部改訂)
本剤の投与により患者の血中にADAMTS13に対するインヒビターが発現するおそれがあり、本剤の効果が得られない可能性がある。国際共同臨床試験において、本剤に対する中和抗体(インヒビター)を発現した患者は認められなかった。本剤が投与された先天性血栓性血小板減少性紫斑病患者76名中17名にて、ADAMTS13に対する低力価の結合抗体が認められたが、有効性及び安全性への臨床的な影響はなく、抗体価の経時的増加も認められなかった。
【15.1臨床使用に基づく情報】(追記)
本剤と中和抗体(インヒビター)発現との因果関係は確立していないが、海外製造販売後において、ADAMTS13に対する中和抗体(インヒビター)を発現した小児の先天性血栓性血小板減少性紫斑病患者1名で死亡が認められたとの報告がある。
効能効果
先天性血栓性血小板減少性紫斑病。
用法用量
本剤を添付の溶解液5mLで溶解し、2~4mL/分の速度で緩徐に静脈内に注射する。
定期的に投与する場合、通常、1回40国際単位/kgを隔週投与するが、患者の状態に応じて1回40国際単位/kgを週1回投与することができる。
急性増悪時に投与する場合、通常、1日目に1回40国際単位/kg、2日目に1回20国際単位/kg、3日目以降は1日1回15国際単位/kgを投与する。
(用法及び用量に関連する注意)
7.1. 定期的に投与する場合の投与頻度は、血小板数、臨床症状、前治療の投与頻度等により決定すること。
7.2. 急性増悪時に投与する場合、投与期間は、血小板数、臨床症状等により決定し、漫然と投与を継続しないこと〔17.1.1参照〕。
警告・禁忌・相互作用・その他の注意
(禁忌)
本剤の成分に対し重篤な過敏症の既往歴のある患者。
(重要な基本的注意)
8.1. 本剤の投与は、血液疾患や血液凝固異常症の治療に十分な知識及び経験を持つ医師の監督のもとで開始すること。
(特定の背景を有する患者に関する注意)
(妊婦)
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
(授乳婦)
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。
(適用上の注意)
14.1. 薬剤調製時の注意
14.1.1. 他の製剤と混合しないこと。
14.1.2. 本剤及び添付溶解液のバイアルが室温に戻っていることを確認すること。
14.1.3. 本剤及び添付溶解液のバイアルキャップを外した後、ゴム栓を消毒し、必ずゴム栓中央部分に添付の専用溶解器(薬液用両刃針)を刺し、溶解すること(薬液濃度は300国際単位/mLとなる)。
14.1.4. 薬液の調製後は3時間以内に使用すること(また、溶解後3時間以内に使用しなかった場合は廃棄すること)。
14.1.5. 本剤の1回の投与につき複数バイアルを要する場合には、バイアルごとに新たな添付の専用溶解器(薬液用両刃針)を使用して溶解すること(使用済みの専用溶解器(薬液用両刃針)は再使用せずに廃棄すること)。
14.1.6. 薬液は添付の専用溶解器(薬液用両刃針)を使用してバイアルからシリンジに移すこと。
14.2. 薬剤投与時の注意
沈殿や変色が認められるものは使用しないこと。
(その他の注意)
15.1. 臨床使用に基づく情報
15.1.1. 本剤の投与により患者の血中にADAMTS13に対するインヒビター発現するおそれがあり、本剤の効果が得られない可能性がある。国際共同臨床試験において、本剤に対する中和抗体(インヒビター)を発現した患者は認められなかった。本剤が投与された先天性血栓性血小板減少性紫斑病患者76名中17名にて、ADAMTS13に対する低力価の結合抗体が認められたが、有効性及び安全性への臨床的な影響はなく、抗体価の経時的増加も認められなかった。
15.1.2. 本剤と中和抗体(インヒビター)発現との因果関係は確立していないが、海外製造販売後において、ADAMTS13に対する中和抗体(インヒビター)を発現した小児の先天性血栓性血小板減少性紫斑病患者1名で死亡が認められたとの報告がある。
(取扱い上の注意)
20.1. 凍結を避け、2~8℃で冷蔵保存すること(やむを得ず冷蔵保存できない場合には、凍結を避け、室温で使用期限を超えない範囲で最長6ヵ月間保存することができるが、再び冷蔵庫に戻さないこと)。
20.2. 直射日光を避けるため、外箱に入れて保存すること。
(保管上の注意)
2~8℃で保存。
副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には、投与を中止するなど、適切な処置を行うこと。
11.1. 重大な副作用
11.1.1. ショック、アナフィラキシー(頻度不明)。
11.2. その他の副作用
1). 血液:(2%未満)血小板増加症。
2). 消化器:(2~5%未満)悪心、(2%未満)便秘、腹部膨満。
3). 精神神経系:(2%未満)頭痛、傾眠、浮動性めまい。
4). 臨床検査:(2%未満)ADAMTS13活性異常。
5). その他:(2~5%未満)熱感、(2%未満)疲労。
薬物動態
16.1 血中濃度
16.1.1 単回投与
(1)国際共同第I相臨床試験(281101試験)
成人の先天性血栓性血小板減少性紫斑病(TTP)患者(日本人を含む)を対象に、本剤20U/kg又は40U/kgを単回静脈内投与した際のADAMTS13活性の薬物動態パラメータは次の通りであった。
ADAMTS13活性の薬物動態パラメータ
<<表省略>>
(2)国際共同第III相臨床試験(281102試験)
成人及び12歳以上の小児の先天性TTP患者(日本人を含む)を対象に、本剤40IU/kgを単回静脈内投与した際のADAMTS13活性の薬物動態パラメータは次の通りであった。
ADAMTS13活性の薬物動態パラメータ
<<表省略>>
16.1.2 反復投与
成人及び小児の先天性TTP患者(日本人を含む)から得られたADAMTS13活性データを用いて母集団薬物動態解析を行った。成人及び小児の先天性TTP患者に本剤40IU/kgを隔週又は週1回で静脈内投与した際の定常状態におけるADAMTS13活性の薬物動態パラメータの母集団薬物動態解析に基づく推定値は次の通りであった。
ADAMTS13活性の薬物動態パラメータ
<<表省略>>
16.8 その他
本剤を臨床の推奨用量で先天性TTP患者に静脈内投与したところ、VWF活性を示すVWF:リストセチンコファクター活性及びVWF抗原は1~2日間、一過性にベースラインから15~25%低下した。
臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国際共同第III相臨床試験(281102試験)
成人及び小児の先天性TTP患者(0~70歳)注1)を対象に定期補充療法及び一時補充療法における有効性及び安全性を検討する前向き、無作為化、対照、非盲検、多施設共同試験を実施した。
注1)2歳未満の先天性TTP患者は組み入れられなかった。
(1)定期補充療法(定期的な投与)
定期補充療法コホートでは各6ヵ月間の第1期及び第2期のクロスオーバー期にて本剤40IU/kg又は標準治療(血漿製剤)を隔週又は週1回投与した。その後、6ヵ月間の第3期にて本剤40IU/kgを隔週又は週1回投与した。日本人5例を含む48例(うち12歳未満の小児8例注2))が無作為化され、日本人5例を含む46例(うち12歳未満の小児8例注2))が試験を完了した注3)。本剤群では第1期から第3期を通じて急性TTPイベントは認められなかったが、標準治療群では第1期に急性TTPイベントが1例に認められた。本剤群では第1期及び第2期に亜急性TTPイベントが1例(1件)、第3期において3例(3件)認められ、第3期の2例に本剤の追加投与が行われた。標準治療群では第1期及び第2期に6例(7件)に亜急性TTPイベントが認められ、4例に標準治療の追加投与が行われた。
次表に示す通り、第1期と第2期において、腎機能障害を除く個別のTTP症状の本剤群での発現率は、標準治療群に比べて低かった。
注2)第1期に、本剤投与を受けた4例、標準治療薬(血漿製剤)投与を受けた4例
注3)最終解析は、定期補充療法コホートに組み入れられた全例が第3期を完了した時点で実施された。なお、中間解析は、定期補充療法コホートの12歳以上の患者の計32例が第3期を完了した時点で、定期補充療法コホート及びオンデマンド療法コホートに組み入れられた全患者を対象に実施された。
第1期及び第2期における有効性の結果(最終解析結果)
<<表省略>>
第1期及び第2期における副作用の発現頻度は、本剤群で4.3%(2/47)、標準治療群で45.8%(22/48)であった。本剤群にて認められた副作用は便秘、ADAMTS13活性異常、頭痛(各1例)であった。第3期における副作用の発現頻度は本剤群で2.2%(1/46)であり、悪心、頭痛(各1例)であった。
(2)一時補充療法(急性増悪時の投与)
一時補充療法コホートには、急性TTPイベントが認められた6例(うち日本人0例、12歳未満の小児1例注12))が登録された。6例のうち2例は本剤による一時補充療法注13)、4例は標準治療(血漿製剤)を受けた。本剤による一時補充療法を受けた急性TTPイベント2件(2例)はいずれも回復注14)した。[7.2参照]
副作用は本剤群で認められなかったが、標準治療群で4例中2例に認められた。
注12)標準治療薬(血漿製剤)投与を受けた。
注13)一時補充療法:初回投与量として1日目40IU/kg、2日目20IU/kg、3日目以降からTTPイベントの回復後2日目まで15IU/kgを連日投与
注14)血小板数が150,000/μL以上又はベースライン値の75%以上であり、かつLDHがベースライン値又は基準値上限の1.5倍以下を回復と定義
17.1.2 国際共同第III相継続投与試験(3002試験)
成人及び小児の先天性TTP患者(0~70歳)注)を対象に、本剤の安全性及び有効性を評価する前向き、非盲検、多施設共同、単群、継続投与試験を実施した。日本人6例を含む75例(うち12歳未満の小児12例、46例は281102試験を完了後に参加)が本剤40IU/kgを隔週又は週1回投与による定期補充療法を受けた。急性TTPイベントは1例(1件)に認められ、亜急性TTPイベント及び個別のTTP症状の発現率は281102試験での本剤群と同程度であった。本剤の曝露期間の中央値(最小値,最大値)は16.9(0.5,33.2)ヵ月であった。
副作用の発現頻度は8.0%(6/75)であり、熱感、悪心(各2例)、腹部膨満、浮動性めまい、疲労、血小板増加症、振戦(各1例)であった。
注)2歳未満の先天性TTP患者は組み入れられなかった。
薬効薬理
18.1 作用機序
ADAMTS13は、亜鉛メタロプロテイナーゼであり、超高分子量VWF多量体を切断し、小単位とすることにより、VWFと血小板との結合及びそれに続く微小血栓の形成を抑制する。本剤は遺伝子組換えADAMTS13であり、本剤によりADAMTS13を補充し、血漿中のADAMTS13活性を回復させることで、血小板減少症につながる微小血管の血栓形成を抑制すると考えられる。
18.2 先天性TTPモデルに対する作用
先天性TTPモデルである遺伝子組換えVWF(rVWF)誘発性ADAMTS13ノックアウトマウスにおいて、本剤は、rVWF投与前に投与することによりTTP様症状の発症を抑制し、rVWF投与後に投与することによりTTP様症状の改善傾向を示した。
18.3 微小血管血栓症の発症抑制効果及び治療効果
先天性TTPモデルであるrVWF誘発性ADAMTS13ノックアウトマウスにおいて、本剤は、rVWF投与前に投与することにより微小血管血栓症の発症を抑制し、rVWF投与後に投与することにより脳血管内で発生した血栓又は形成中の血栓を消失させた。
18.4 内因性VWF多量体の切断作用
ラット及びカニクイザルを用いた反復投与毒性試験において、本剤の投与後に内因性VWF多量体の切断が認められた。
類似した薬効の薬
医師の処方により使用する医薬品。



 で医薬品を比較する
で医薬品を比較する
